Autores
Dra. Marta Luján Kura; Dra. María Belén Campagno (Hospital Militar Central, Capital Federal, Argentina)
INTRODUCCIÓN
El estudio con Doppler color (DC) es un método no invasivo y reproducible que permite conocer el estado anatómico y funcional de las venas de los miembros inferiores. El objetivo de este trabajo es realizar una revisión y actualización de esta técnica en cuanto a la metodología de examen y las patologías prevalentes factibles de ser evaluadas con ella.
ANATOMÍA
El sistema venoso de los miembros inferiores se divide en profundo, superficial y de las venas perforantes.
Sistema venoso profundo. Se encuentra por debajo de la aponeurosis muscular (subfascial). En la región suprapatelar está formado por una vena que acompaña a una arteria, que lleva el mismo nombre. El sistema se compone por la vena femoral común, que drena en la iliaca externa a la altura de la arcada inguinal, y está conformada por la afluencia de la femoral superficial y la femoral profunda. Esta última se origina de la confluencia de las venas de drenaje de los músculos laterales y posteriores del muslo.
La vena femoral superficial, por su parte, se origina de la vena poplítea, en el margen superior de la fosa homónima y cursa en el canal femoral (el término “femoral superficial” no está autorizado por la nueva nomenclatura para evitar confusiones con el sistema superficial, y se la denomina solamente como “vena femoral”) (1, 2).
Pueden existir variantes de la vena femoral (3). La más frecuente es la duplicación, presente en un 8 a 10% de la población general, que puede ser: completa, cuando la duplicación se extiende hasta la vena femoral común; distal, cuando drena en el tercio medio; proximal, cuando la duplicación drena a la vena femoral común; compleja, cuando la femoral está duplicada en más de dos ramas; y duplicación de poplítea propiamente dicha.
Conocer estas variantes adquiere importancia en el momento del diagnóstico de las trombosis y de las insuficiencias (3).
En la región infrapatelar existen dos venas que acompañan a cada arteria; estas son las tibiales posteriores, las tibiales anteriores y las peróneas.
En el espesor de los músculos de los miembros inferiores existen venas musculares que drenan durante la sístole muscular (contracción muscular) hacia la vena poplítea y el tronco tibioperoneo: son los senos venosos soleos y gemelares (mediales y laterales) que, a diferencia del resto de las venas sistémicas, no presentan sistema valvular y su funcionamiento depende de la contracción muscular (bomba veno-muscular).
Sistema venoso superficial. Está formado por la vena safena mayor (término que reemplaza a “safena interna”) y la vena safena menor (llamada antes “safena externa”). Ambas transcurren por la pierna y el muslo en el compartimento safena, limitado por la fascia superficial hacia la parte anterior y la fascia muscular hacia la posterior (1, 2, 3) (Fig. 1).
Existen también venas safenas accesorias que desembocan en la femoral común. La safena accesoria anterior recorre la cara anterior del muslo y la accesoria posterior, la región posterior; esta última se inicia a la altura de la pierna, donde se denomina “vena de Leonardo”. También hay otras venas tributarias de la safena mayor o accesorias; estas son la vena circunfleja anterior, que asciende oblicua en la región anterior del muslo, y la vena circunfleja posterior, que asciende también oblicua en la región posterior del muslo (Fig. 2).
Sistema de venas perforantes. Son vasos de un diámetro que no debe superar los 3 mm. Atraviesan la aponeurosis muscular y comunican el sistema venoso superficial con el sistema venoso profundo, mediante un sistema valvular que en condiciones normales permite el drenaje de sangre en ese sentido. La forma de cono truncado, con el orifico externo menor que el interno favorece direccionar el flujo desde el sistema superficial al profundo (4) (Fig. 3 y Fig. 4).
Las venas perforantes se diferencian en: directas, que comunican el sistema venoso profundo con las venas safenas; e indirectas, que lo comunican con alguna vena tributaria. Cuando se invierte el flujo de la perforante por in-suficiencia venosa, se denominan “perforantes de fuga”, esta es una condición anormal, que requiere tratamiento, las perforantes de reentrada compensan a las de fuga, tienen dirección normal (4).
Las venas perforantes se encuentran distribuidas en las siguientes regiones: posterior del glúteo, anterior y laterales del muslo, a la altura de la rodilla, en la pierna, en el tobillo y en el pie. En la Fig. 5 se muestran los cinco grupos de perforantes más frecuentes (1, 2, 5, 6).
Las venas tributarias o comunicantes también forman parte del sistema superficial (comunican venas superficiales entre sí), y se ubican anatómicamente en la topografía subdérmica y epifascial. Una variante bastante frecuente es la prolongación axial del cayado de la vena safena menor (antes llamada “vena de Giacomini”), que se dirige por la región posterior del muslo hasta su tercio medio y luego asciende medialmente hasta desembocar en la vena safena mayor (7, 8).
TROMBOSIS VENOSA PROFUNDA
La trombosis venosa profunda (TVP) tiene una incidencia del 0,2%. Se asocia a venas varicosas, cáncer, embarazo-posparto, anticonceptivos orales, inmovilidad, cirugía y trombofilia venosa congénita (7). Clínicamente se manifiesta con dolor, tumefacción, edema y cianosis del miembro inferior (Fig. 6).
Para la exclusión, el diagnóstico de la TVP y los diagnósticos diferenciales es seguro y efectivo el uso del ultrasonido (US), el dímero-D y la evaluación de la puntuación de Wells. Alrededor del 20 al 40% de los pacientes con TVP desarrolla un síndrome postrombótico (8). Para el diagnóstico de TVP proximal (por encima de la rodilla) el DC tiene un valor predictivo del 95%, con una sensibilidad mayor al 95% y una especificidad del 97%. En las TVP agudas por debajo de la rodilla la sensibilidad cae significativamente, hasta el 70 a 80% (9).
El trombo se origina en una zona de estancamiento, como la región de la base de la cúspide valvular, y una vez formado se propaga a lo largo de la luz venosa. En algunos casos la luz solo se llena parcialmente, mientras que en otros se ocluye. Durante la fase aguda se induce a la inflamación de la pared venosa y provoca una flebitis, que es causante del dolor espontáneo. De 7 a 14 días después de producida la reacción inflamatoria se resuelve, y el trombo residual que no fue listado por acción del plasminógeno se transforma en tejido fibroso.
El diagnóstico de TVP se realiza en modo B, median-te compresiones intermitentes cada 2 o 3 cm en el eje transverso y en todo el trayecto del vaso. No debe realizarse en el eje longitudinal debido a que las venas pueden desplazarse fuera del plano de la imagen y simular que se ha comprimido.
Clasificación de la TVP
Esta se determina según el tiempo de evolución en relación a la visualización con DC (9, 10) (Fig. 7, Fig. 8).
TVP aguda
Hallazgos en la imagen con modo B:
- Baja ecogenicidad.
- Distensión venosa.
- Pérdida de compresibilidad.
- Trombo que flota libremente: cuando se observa esta imagen no se debe manipular distalmente porque este es potencialmente embolígeno.
Anomalías en la señal DC:
- Ausencia de flujo proximal al segmento trombosado.
- Distal al mismo se observa flujo continuo, con ausencia de variabilidad respiratoria.
- Colateralización: las venas colaterales aumentan rápidamente de tamaño durante la fase aguda.
- Las imágenes con flujo color se realizan en el eje largo paralelo a las venas.
TVP subaguda (2 semanas a 6 meses)
Hallazgos en la imagen con modo B:
- Aumento de la ecogenicidad.
- Reducción del trombo y tamaño de la vena: con la lisis del trombo la vena se distiende menos y vuelve a su calibre normal.
- Adherencia del trombo: no se visualiza trombo flotando libremente.
- Reanudación del flujo.
- Colateralización: continúan aumentando de tamaño.
| Tabla 1. Diagnósticos diferenciales de edema agudo | ||
| Unilateral | Bilateral | |
| Etiología | TVP | Insuficiencia renal, cardíaca, hepatopatía. |
| Tipo de edema | Duro, doloroso, empastamiento muscular, cianosis. | Blando, indoloro, liso. |
| Examen solicitado | DC | Perfil renal, lipídico, cardíaco. |
| Tabla 2. Diagnósticos diferenciales de edema crónico | ||||
| Unilateral | Bilateral | |||
| Etiología | Isquemia | Insuficiencia venosa crónica | Linfedema | Lipedema |
| Tipo de edema | Blando, doloroso, frío, necrosis | Duro, dermatitis ocre pigmentaria. Atrofia blanca | Blando, blanco Afecta muslo pierna, pie, dedos del pie | Blando, a veces doloroso, afecta muslo y pierna; respeta pie y dedos del pie “Collares de grasa” |
| Examen solicitado | DC Índice tobillo/ braquial |
Doppler flebografía | Linfografía | Perfil endocrinológico |
TVP crónica (más de 6 meses)
Hallazgos en la imagen con modo B:
- Engrosamiento de la pared.
- Material intra-luminal ecogénico.
- Cordón fibroso: disminución del calibre y aumento de la ecogenicidad que algunas veces puede desaparecer la imagen ecográfica de la vena.
- Anomalía en válvulas: lesión de las valvas por engrosamiento de las cúspides, adherencia de la cúspide a la pared venosa y pérdida de movilidad y falta de aposición de las cúspides en el centro del vaso. Como consecuencia, hay reflujo y estasis venosa persistente.
El diagnóstico diferencial del paciente con TVP se basa fundamentalmente, en poder discernir clínicamente entre los distintos tipos de edema. De esta forma, la práctica con DC es simplemente la confirmación de la presunción clínica. En el análisis clínico se deben completar una serie de preguntas, en el siguiente orden:
- ¿Cuál es la duración del edema? si el tiempo de evo-lución es menor a 72 horas es agudo y en este caso el primer diagnóstico probable será TVP.
- ¿Es doloroso?, la TVP causa dolor, en tanto que el linfedema y el lipedema son indoloros.
- ¿Toma medicación que bloquea los canales cálcicos? es decir, drogas antinflamatorias, prednisona (10, 11, 12, 13, 14).
- ¿Existe historia de enfermedades sistémicas (cardíaca, hepática, renal)?
- ¿El paciente tiene antecedentes de tumor abdominal o pelviano, radioterapia?
En las tablas 1 y 2 se representa una síntesis de los diagnósticos diferenciales que se deberán tener en cuenta, previo a la evaluación con DC.
Complicaciones de la TVP
La TVP puede recanalizarse y ocasionar una secuela local, o desprenderse y generar la complicación más grave: el trombo embolismo pulmonar; el 70% de estos casos sintomáticos presentan trombosis venosa profunda concomitante.
La TVP, a pesar de la recanalización, produce daños en la pared y en el sistema valvular de las venas que ocasionan inmovilización de las válvulas en el 60% de los casos, con la consiguiente incompetencia y reflujo en bipedestación. En el DC se observan bandas fibrosas en el interior del vaso con señal vascular fragmentada (Fig. 9).
La hipertensión venosa que se ocasiona se manifiesta clínicamente como un edema crónico de la pierna, hiperpigmentación en el tobillo y, por último, ulceración por encima del tobillo; estos cambios son conocidos como “síndrome post trombótico”(14).
INSUFICIENCIA VENOSA
Para comprender la insuficiencia venosa es necesario conocer la fisiología. Un componente fundamental en la anatomía de las venas lo constituyen las válvulas venosas, que son pliegues de colágeno en forma de semiluna recubiertas de endotelio que salen de la pared de la vena. Presentan dos valvas, llamadas “cúspides”, con dos bordes libres hacia la porción medial de la vena (Fig. 10).
Las válvulas son más numerosas en la pierna distal y disminuyen hacia la cadera. En las extremidades inferiores, las válvulas funcionan para dividir la columna hidrostática de la sangre en segmentos, y para asegurar el flujo de superficial a profundo y de caudal a craneal. Las cúspides de la válvula de las extremidades inferiores permanecen abiertas durante el reposo en posición supina. El cierre de la válvula es un evento iniciado por inversión pasiva del gradiente de presión transvalvular anterógrada en reposo.
A medida que el gradiente de presión se invierte, hay un corto período de flujo retrógrado, o reflujo, hasta que el gradiente se hace suficiente para causar el cierre de la válvula. Por lo tanto, el cierre de la válvula requiere, primero, el cese de flujo anterógrado, seguido de un breve intervalo de flujo retrógrado de velocidad suficiente para coaptar completamente las cúspides (Fig.11) (16). En condiciones de normalidad valvular, con la persona en posición vertical, el reflujo dura menos de 0,5 segundos (Fig. 12), y si este persiste más de 0,5 segundos se define como “reflujo patológico” (Fig. 13).
Para un adecuado funcionamiento, el sistema venoso debe estar permeable, el sistema valvular y el sistema muscular indemne, y la función cardíaca conservada. Cuando algunos de estos factores fallan se ocasiona una alteración en el retorno venoso, con la consiguiente dilatación vascular, incompetencia valvular y posterior insuficiencia venosa.
El término “insuficiencia venosa” se refiere a la in-competencia valvular que permite la inversión del flujo y favorece la hipertensión venosa en los segmentos distales. Puede ser de origen primario o secundario al mal funcionamiento valvular postrombótico.
La insuficiencia superficial se puede describir como un shunt veno-venoso o un circuito retrógrado, que está constituido por un punto de fuga, que puede ser la unión safeno-femoral o alguna perforante de fuga, un trayecto varicoso (de flujo retrógrado), y un punto de reentrada al sistema venoso profundo a través de las venas perforantes (16, 17, 18).
La valoración de la patología varicosa comienza con la visualización de los miembros inferiores para poder, de esta manera, clasificar clínicamente la patología, va-lorar los cambios tróficos de la piel y la presencia de úlceras. (Fig. 14, Fig. 15) (19). La CEAP clasifica la insuficiencia venosa en base a la clínica, etiopatogenia, anatomía pato-lógica y fisiopatología (Tabla 3) (20).
En el examen con DC de los miembros inferiores primero se estudiará el paciente en decúbito dorsal, para evaluar la permeabilidad del sistema venoso. Luego, si el paciente no presenta trombosis, se lo estudiará en bipedestación, si es posible sobre una tarima con baranda, y se utilizará una regla milimetrada de al menos 60 cm, para medir desde la base del pie la distancia en la que está la perforante insuficiente; si existe algún impedimento físico para que permanezca de pie se lo ubicará sentado con las piernas sin apoyo. De esta manera se favorece el incremento de la presión hidrostática, a fin de realizar una correcta evaluación de la competencia valvular y un mapeo venoso.
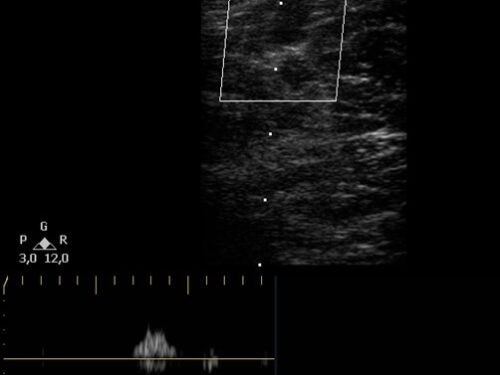
La evaluación comienza desde la región inguinal, utilizando un transductor lineal con una frecuencia de 7-11MHz. En modo B se visualiza la unión safeno-femoral y, realizando un corte longitudinal, se mide el diámetro anteroposterior del cayado, situado entre la válvula ostial y preostial (Fig. 16). Posteriormente se le solicita al paciente que realice la maniobra de Valsalva o se comprime la región gemelar y se valora mediante DC para corroborar la adecuada competencia valvular. Así se continúa el estudio, con cortes transversos y siguiendo el recorrido de la vena safena mayor, las tributarias y las venas perforantes, realizando compresiones distales cada 3 a 5 cm (Fig. 17).
El reflujo fisiológico, que se ve representado como inversión del color o de la onda de Doppler pulsado, no debe superar un segundo en el sistema venoso profundo y el cayado safeno-femoral, y los 0,5 segundos en el sis-tema venoso superficial. Los diámetros venosos deben ser como máximo de 6 mm en topografía suprapatelar y de 3 mm infrapatelar, y las venas perforantes no deben superar los 3 mm.
Es importante señalar la longitud de la insuficiencia, así como determinar el origen (por perforante insuficiente, tributarias insuficientes o ectasias venosa) y su sitio de drenaje (perforante, tributarias), o si simplemente disminuye su calibre y se vuelve competente. También existen insuficiencias focales que pueden no tener causa aparen-te, y así debe informarse, indicando la distancia del piso en que se encuentra, debido a que pueden ser el origen de una futura insuficiencia. El mapeo venoso es de utilidad para el cirujano vascular, para una correcta visualización gráfica de lo detallado en el informe.
Se dibujan las venas perforantes y comunicantes insuficientes que presenten un diámetro mayor a 3,5 mm, más una evaluación de la dirección del flujo para determinar si son de fuga o de reentrada, y la presencia de reflujo al Doppler pulsado. Se mide la distancia desde el piso hasta el sitio donde perfora la aponeurosis o donde drena en la vena principal, en caso de ser tributaria; tam-bién se pueden agregar las teleangiectasias, venas tegumentarias, úlceras o cambios tróficos en la piel (Fig. 18). Se utiliza el color azul para indicar las venas competentes y el rojo para las insuficientes (17, 18).
RECIDIVA DEL PACIENTE OPERADO
En la valoración de la recidivas es importante tener en cuenta a las venas accesorias, la neoformación de vasos en la topografía del cayado, medir el remanente del cayado de la safena mayor, la presencia de duplicaciones o hipoplasias preexistentes al momento de la cirugía o que pueden reaparecer en los postquirúrgicos, debido a que la morfología habitual cambia y valorar la presencia de perforantes en la topografía de la safena menor (19, 20, 21, 22).
CONCLUSIÓN
El DC venoso es un método muy útil, con una sensi-bilidad del 100% y una especificidad del 62% al 83% para el diagnóstico de la insuficiencia venosa. Combinado con un buen examen clínico es una excelente herramienta para el diagnóstico de pacientes varicosos. Permite una valoración topográfica y hemodinámica del paciente con IVC, sobre todo determinar el punto exacto donde las venas perforantes atraviesan la fascia muscular. Esto fa-cilita la ligadura de todas las perforantes incompetentes, posibles así de realizar con pequeñas incisiones y redu-ciendo el tiempo de intervención, las complicaciones quirúrgicas y la persistencia o recidiva precoz de las varices. También aumenta la autonomía de los profesionales, su capacidad de acierto y su seguridad en el manejo de la enfermedad tromboembólica venosa.
Un estudio dedicado, con un adecuado conocimiento de la anatomía y la correcta nomenclatura tiene particular importancia al momento de diseñar el informe, ya que eso le permitirá al flebólogo una correcta interpretación del mapeo venoso, así como un menor grado de complicaciones y, especialmente, recidivas postquirúrgicas.
Bibliografía
- Gómez C, Jiménez H, Ulloa JH: “Nomenclatura de las venas de los miembros inferiores y términos en flebología: los consensos internacionales”, Rev Colomb Cir, 2012, 27, 139-145.
- Caggiati A, Bergan J, et al.: “Nomenclature of the veins of the lower limbs: International Interdisciplinary Consensus Committee on Venous Anatomical Terminology”, J Vasc Surg, 2002, 36, 416-22.
- Román-Guzmán E, et al.: “Variantes anatómicas del sector fémoro-poplíteo”, Rev Mex Angiol, 2014, 42, 2, 86-90.
- Eklof B, Rutherford RB, Bergan JJ, et al.: “Revisión de la clasificación CEAP de la enfermedad venosa crónica”, J Vasc Surg, 2004, 40, 1248-52.
- Pellerito J, Polak JF: Introduction to Vascularb Ultrasonography, 6° ed., 2012, Elsiever.
- Bundens WP, Bergan JJ, Halasz NA, Murray J, Drehobl M.: “The superficial femoral vein: a potentially lethal misnomer”, JAMA 1995, 274, 1296-8.
- Bergan JJ.: “Editor’s note”, Venous digest, 1999, 6, 5b.
- Allan PL, Dubbins PA, Pozniak MA, McDicken WN: 2° ed., 2008, Elsevier.
- Caggiati A, et al.: “Nomenclature of the veins of the lower limbs: An international interdisciplinary consensus statement”, Journal of Vascular Surgery, 2002, vol. 36, iss. 2, 416-422.
- Ely JW, Osheroff JA, Chambliss ML: “Approach to Leg Edema of Unclear Etiology”, J Am Board Fam Med, 2006, vol. 19, n° 2, march-april, 148-160.
- Gorman WP, Davis KR, Donnelly R: “ABC of arterial and venous disease. Swollen lower limb-1: general assessment and deep vein thrombosis”, BMJ, 2000, 320, 1453-6.
- Ciocon JO, Fernández BB, Ciocon DG: “Leg edema: clinical clues to the differential diagnosis”, Geriatrics, 1993, 48: 34-40.
- Young JR: “The swollen leg. Clinical significance and differential diagnosis”, Cardiol Clin, 1991, 9, 443-56.
- Gloviczki P: “The care of patients with varicose veins and associated chronic venous diseases: Clinical practice guidelines of the Society for Vascular Surgery and the American Venous Forum”, Journal of Vascular Sourgery, 2011, 53, 5, 2-48.
- Meissner MH: “Lower Extremity Venous Anatomy”, Semin Intervent Radiol, 2005, 3, 147-156.
- http://mmegias.webs.uvigo.es/2organosa/guiada_o_a_05 cardiovascular.php
- Meissner MH, Gloviczki P, Bergan J, Kistner RL, Morrison N, Pannier F, Pappas PJ, Rabe E, Raju S, Villavicencio JL: “Primary chronic venous disorders”, J Vasc Surg, 2007, 46, supl. S, 54S-67S.
- Michiels JJ, Moosdorff W, Maasland H, Michiels JM, Lao MU, Neumann HA, Dulicek P, Stvrtinova V, Barth J, Palareti G: “Duplex ultrasound, clinical score, thrombotic risk, and D-dimer testing for evidence based diagnosis and management of deep vein thrombosis and alternative diagnoses in the primary care setting and outpatient ward”, International Angiology Journals, 2014, 33, 1, 1-19.
- Zwibel WJ, Pellerito JS: Dopppler general. 5° ed. Marban, 2008.
- Polak JP: Doppler cuello y extremidades. 2° ed. Marban, 2007.
- Meissner MH: “Anatomía venosa de las extremidades inferiores”, Seminario Intervencionismo Radiológico, 2005, 22, 147-156.
- Cura JL, Pedraza S, Gayete A: Radiología esencial. Sociedad Española de Radiología, Panamericana, 2010.