Autor: Dr. Renzo Eduardo Gómez Cubides (Hospital General de Agudos “José María Ramos Mejía”)
Directora de la tesis: Dra. Marta Kura
Padrino de la tesis: Dr. Sebastián Facundo Pérez Espinosa
Resumen
El objetivo de este estudio fue evaluar el rendimiento diagnóstico de las punciones de nódulos mamarios clasificados como BI-RADS 4 visibles por ecografía en el Hospital General de Agudos “José María Ramos Mejía”, entre el 31 octubre de 2022 y el 31 octubre de 2024. Este trabajo revisa los resultados de biopsias realizadas en pacientes con nódulos BI-RADS 4, comparando los hallazgos ecográficos con el diagnóstico histopatológico obtenido a través de la punción. Los resultados del análisis de biopsias ecodirigidas en pacientes con lesiones mamarias BI-RADS 4 reveló una distribución de lesiones benignas (56%) y malignas (44%) en una muestra de 50 pacientes. Las lesiones benignas se observaron mayormente en mujeres jóvenes (edad promedio de 36,8 años), mientras que las malignas predominaron en mujeres mayores (promedio de 48,5 años). La sensibilidad y especificidad de este diagnóstico fueron evaluadas, mostrando un rendimiento diagnóstico moderado, con 50% de precisión tanto en la identificación de lesiones malignas como en la exclusión de lesiones benignas permitiendo identificar la precisión, sensibilidad, especificidad, y los valores predictivos de este método en la población estudiada, proporcionando evidencia sobre su efectividad en el diagnóstico temprano de lesiones malignas en mama. Estos resultados sugieren la necesidad de mejorar la precisión en el diagnóstico, a pesar de la utilidad de la ecografía y la biopsia en la práctica clínica.
Palabras clave: carcinoma, examen clínico, biopsia por aspiración con aguja fina, mamografía, ultrasonografía, cáncer de mama, nódulos mamarios, BI-RADS.
Introducción
Las lesiones mamarias son una de las principales preocupaciones de salud en mujeres de todas las edades. La ecografía mamaria se ha consolidado como una herramienta clave en el diagnóstico precoz de estas lesiones, permitiendo su clasificación en el sistema BI-RADS (Breast Imaging Reporting and Data System). Las lesiones BI-RADS 4 son aquellas con una alta sospecha de malignidad, que requieren confirmación mediante procedimientos invasivos, como la biopsia ecodirigida.
El Hospital General de Agudos “José María Ramos Mejía”, al ser un centro de referencia, realiza este tipo de estudios con el fin de mejorar el diagnóstico y tratamiento de las pacientes. La biopsia ecodirigida es fundamental para confirmar la naturaleza benigna o maligna de las lesiones, permitiendo intervenciones oportunas. Sin embargo, los resultados de estos estudios pueden tener implicaciones significativas en la precisión diagnóstica, lo que justifica la evaluación de su rendimiento.
Este estudio tiene como objetivo analizar el rendimiento diagnóstico de las punciones de nódulos mamarios BI-RADS 4 visibles por ecografía y de tal manera evaluar la sensibilidad y especificidad de las biopsias ecodirigidas en pacientes con lesiones mamarias clasificadas como BI-RADS 4, que fueron sometidas a procedimientos diagnósticos en el mencionado hospital entre 2022 y 2024.
Diagnóstico
El cáncer de mama es una de las principales causas de muerte en mujeres a nivel mundial y su diagnóstico temprano es crucial para mejorar los resultados clínicos y la supervivencia. La clasificación BI-RADS, desarrollada por el American College of Radiology (ACR), es una herramienta ampliamente utilizada en la evaluación de lesiones mamarias. Dentro de esta clasificación, los nódulos categorizados como BI-RADS 4 presentan una sospecha intermedia de malignidad, con un rango de probabilidad de entre el 2% y el 95%, lo que los convierte en candidatos para una evaluación diagnóstica exhaustiva mediante biopsia.
En el contexto del Hospital General de Agudos “José María Ramos Mejía”, la ecografía es una técnica de imagen accesible y de primera línea para la evaluación de estos nódulos en mujeres con mamas densas, o como complemento de la mamografía. La punción ecoguiada es una técnica de elección para obtener tejido de estos nódulos y confirmar o descartar malignidad. Sin embargo, es necesario evaluar de manera objetiva el rendimiento diagnóstico de este procedimiento en términos de sensibilidad, especificidad en la población atendida en este hospital.
Este diagnóstico permitirá evaluar la efectividad de las punciones ecoguiadas en nódulos BI-RADS 4, contribuyendo a optimizar el proceso de detección y manejo de casos sospechosos de cáncer de mama, mejorando los recursos hospitalarios y reduciendo procedimientos innecesarios para las pacientes.
Objetivos
Objetivo general
Evaluar el rendimiento diagnóstico de las punciones de nódulos mamarios BI-RADS 4 visibles por ecografía en el Hospital General de Agudos “José María Ramos Mejía”.
Objetivos particulares
- Determinar la tasa de malignidad en los nódulos mamarios clasificados como BI- RADS 4.
- Determinar la sensibilidad y especificidad de las punciones ecoguiadas en nódulos mamarios BI-RADS 4, en comparación con el diagnóstico histopatológico obtenido.
- Evaluar la precisión diagnóstica de las punciones guiadas por ecografía.
- Evaluar el impacto clínico de los resultados de las punciones en el manejo de pacientes con nódulos mamarios BI-RADS 4.
Marco teórico y antecedentes
En las primeras civilizaciones, los nódulos mamarios eran observados, pero no comprendidos en términos médicos. En Egipto, por ejemplo, el Papiro de Edwin Smith (aproximadamente, 1600 a.C.) describe casos de tumores en el seno, y se considera uno de los primeros documentos médicos en observar cambios en las mamas, aunque sin una comprensión clara de sus causas o implicancias. En Grecia, Hipócrates describió masas en los senos, relacionándolas con un “exceso de bilis negra”, una teoría de los humores que predominaría hasta la Edad Media.
A finales del siglo XIX y principios del XX, el estudio de las enfermedades mamarias comenzó a avanzar gracias a los progresos en la anatomía patológica. La identificación y descripción de las células cancerosas por Rudolf Virchow fue un gran avance en la comprensión del cáncer de mama. En 1913, el médico alemán Albert Salomon realizó la primera radiografía de un tejido mamario extirpado,(1) lo que permitió una observación inicial de la estructura interna de los nódulos y abrió las puertas al uso de la imagenología en el diagnóstico mamario.
La mamografía como técnica de detección comenzó a establecerse en los años 1950. Robert Egan, radiólogo estadounidense, desarrolló una técnica que incrementó la calidad de las imágenes mamográficas, permitiendo identificar con más precisión los nódulos en el tejido mamario. Su trabajo, «Mammography», publicado en 1960, marcó un hito en el diagnóstico temprano de nódulos mamarios y en la diferenciación entre lesiones benignas y malignas.(2)
En 1993, el American College of Radiology (ACR) desarrolló el Breast Imaging Reporting and Data System (BI-RADS), un sistema estandarizado de clasificación para las imágenes mamarias que permite categorizar los hallazgos según su probabilidad de malignidad. Esto incluye los nódulos mamarios, que son evaluados por su forma, márgenes y otras características imagenológicas.(3) Además, el desarrollo de la ecografía y la resonancia magnética en la evaluación de los nódulos mamarios ha permitido un análisis más detallado y seguro, especialmente en mujeres con mamas densas, donde la mamografía es menos eficaz.
La introducción de la punción y la biopsia guiada por ecografía en los años 1990 y 2000 proporcionó una herramienta mínimamente invasiva para obtener muestras de nódulos sospechosos. Esto ha permitido confirmar diagnósticos y mejorar la precisión de la caracterización de los nódulos mamarios, aumentando así la efectividad de los tratamientos tempranos y reduciendo el número de cirugías innecesarias en lesiones benignas.(4)
Nódulos mamarios
Los nódulos mamarios son masas o lesiones que pueden presentarse en el tejido mamario y abarcan una variedad de condiciones, tanto benignas como potencialmente malignas. Entre los tipos de nódulos mamarios se encuentran los nódulos alveolares hiperplásicos y los nódulos fibrosos, cada uno con características distintas.
- Nódulos alveolares hiperplásicos: son considerados lesiones preneoplásicas en el modelo de tumorigénesis mamaria murina. Se describen como lesiones discretas y morfológicamente identificables que preceden a los tumores mamarios. En ratones, estos nódulos son comunes en aquellos infectados con el virus del tumor mamario o expuestos a ciertos carcinógenos. Se caracterizan por una hiperplasia epitelial intraductal y pueden evolucionar hacia adenocarcinomas mamarios.(5-6)
- Nódulos fibrosos: se identifican frecuentemente en biopsias de núcleo grueso de la mama. Se caracterizan por presentar márgenes circunscritos o indistintos en las imágenes, y aunque pueden sugerir malignidad, son benignos. En los casos revisados, los nódulos fibrosos no presentan calcificaciones y, en la mayoría de los casos, la biopsia repetida confirma su naturaleza benigna.(7)
Es importante destacar que el término “nódulo mamario” es amplio y puede incluir otras entidades, como fibroadenomas, adenomas del pezón y lesiones raras, como la mucinosis nodular de la mama, cada una con sus propias características clínicas y patológicas.(8-9)
Epidemiología
Según la OMS, el cáncer de mama es la principal causa de muerte relacionada con el cáncer en todo el mundo, con un riesgo estimado de por vida del 12%.(10) La enfermedad benigna de la mama suele ser más común, ya que afecta entre el 25% y el 50% de las mujeres adultas y representa el 3% de los encuentros de los médicos generales con pacientes femeninas.(11) La mayoría de estos casos pueden presentarse inicialmente con una nueva masa mamaria. Por lo tanto, todo médico debe tener confianza en la evaluación y el tratamiento de estas pacientes, y un enfoque exhaustivo y consistente lo permite. El enfoque de triple evaluación analizado en este tema ha mejorado los resultados al permitir un diagnóstico oportuno y un enfoque interprofesional coordinado.(12)
Factores de riesgo
El principal factor de riesgo para desarrollar cáncer de mama es la exposición excesiva a estrógenos. Por lo tanto, es esencial interrogar sobre la exposición a estrógenos a lo largo de la vida en todas las pacientes que presentan una nueva masa mamaria. La edad temprana de la menarquia, la edad tardía del primer embarazo, la nuliparidad, los anticonceptivos orales o la terapia de reemplazo hormonal y la menopausia tardía aumentan la exposición a estrógenos, mientras que la lactancia materna es un factor protector.(13)
A los pacientes varones se les debe preguntar sobre tratamientos hormonales previos para el cáncer de próstata, el uso de finasterida o testosterona, episodios de orquitis/epididimitis o síndrome de Klinefelter diagnosticado previamente.(14) Se cree que otros factores de riesgo, como el consumo excesivo de alcohol y la obesidad, aumentan los estrógenos endógenos.(15)
Causas comunes de nódulos mamarios
Fibroadenomas: son tumores benignos provocados por la proliferación de tejido conectivo encapsulado, que pueden encontrarse a cualquier edad, aunque son más frecuentes entre la segunda y tercera década de la vida. Son los tumores mamarios más comunes en las mujeres jóvenes y, si bien suelen ser únicos, hasta un 15% de las pacientes tienen varios nódulos. Generalmente se palpan como una tumoración elástica muy móvil, a veces dolorosa, y que puede cambiar de tamaño y consistencia con el ciclo menstrual en respuesta a la estimulación estrogénica.(16) Su tamaño aumenta en el embarazo y disminuye durante la menopausia (en esta etapa los fibroadenomas también pueden endurecerse como resultado de su calcificación).
Quistes: son formaciones líquidas encapsuladas que se producen por la involución de los lóbulos mamarios y/o la dilatación de los conductos galactóforos. El desarrollo de quistes es común en las pacientes mayores de 40 años. Pueden ser silentes (y detectarse al realizar el examen físico de control) o ponerse de manifiesto porque provocan dolor. Muchas veces es imposible diferenciar un quiste de un nódulo sólido o de un cáncer con el examen físico, por lo que el diagnóstico suele requerir ecografía y/o punción aspiración con aguja fina.(16)
Enfermedad fibroquística de la mama: también conocida como “displasia mamaria”. Ambos términos son ambiguos, dado que incluyen múltiples entidades, que van desde cambios fisiológicos relacionados con el estímulo hormonal hasta lesiones que podrían evolucionar al cáncer de mama. Aunque su uso es desaconsejable, están ampliamente difundidos entre los médicos y las pacientes, y constituyen un motivo frecuente por el cual se solicitan exámenes mamarios y mamografías en forma periódica e innecesaria. La denominación de displasia mamaria suele agrupar a un gran número de entidades mamarias no neoplásicas caracterizadas por cambios anatomopatológicos que llevan a la aparición de tejido conectivo fibroso, nódulos y quistes en el tejido mamario. Sin embargo, estos cambios resultan de una respuesta fisiológica de la mama a los estímulos hormonales. Por esta razón muchos autores sostienen que, en realidad, la displasia mamaria no existe y que estos cambios deben asumirse como parte del desarrollo normal y común de la mama a lo largo de la vida.(16)
Evaluación de un nódulo o masa mamaria
- Interrogatorio: la edad es un factor importante, ya que la chance de que una masa palpable se deba a una enfermedad maligna es cercana a cero a los 25 años; mientras que se aproxima al 75% a los 70 años. En las mujeres con antecedentes familiares (hermana, madre o tía materna) o personales de cáncer de mama, o con antecedentes personales de hiperplasia típica o atípica de la mama, la probabilidad de que una masa palpable sea cáncer es muy alta. Sin embargo, la mayoría de las mujeres con cáncer de mama no tiene antecedentes familiares.(16)
- Examen físico: permitirá determinar si la paciente tiene uno o varios nódulos y las características de estos. Los nódulos duros elásticos, de bordes netos y regulares, móviles, sin adherencia a los planos profundos y dolorosos a la palpación tienen alta probabilidad de ser benignos. Por otro lado, el hallazgo de una masa dura, de bordes irregulares, adherida a la piel y a los planos profundos es muy sugestivo de cáncer de mama. Otros signos asociados a malignidad son la retracción de la piel o del pezón y la secreción sanguinolenta por el pezón. Sin embargo, con frecuencia es difícil distinguir si una masa es atribuible a un cáncer de mama o no lo es utilizando el examen mamario como única herramienta, ya que los signos de alarma que mencionamos tienen una sensibilidad y una especificidad bajas. Por ejemplo, se ha descripto que tres de cada cinco nódulos neoplásicos son móviles, y dos de cada tres tienen bordes regulares a la palpación. La probabilidad de que una masa sea maligna es del 50% si no es móvil y del 14% al 20% si lo es. El examen clínico mamario permite clasificar a las pacientes que consultan porque se palparon un nódulo en dos grandes grupos con diferente riesgo de tener cáncer de mama. La detección de múltiples nódulos es sugestiva de una nodularidad mamaria (cíclica o no), entidad benigna relacionada con la respuesta mamaria a los estímulos hormonales. Por otro lado, el hallazgo de un nódulo aislado o de múltiples nódulos, pero con uno de ellos dominante (es decir, que se destaca por su tamaño o por tener alguna característica distintiva con respecto a los otros: bordes irregulares, adherencia a planos profundos, etc.) es sugestivo de cáncer de mama y los esfuerzos diagnósticos deberán dirigirse a descartar la patología maligna.(16)
Estudios complementarios
- Mamografía: la mamografía es esencial en la evaluación de cualquier nódulo palpable, aun cuando el diagnóstico de cáncer parezca obvio. Quedan exceptuadas las mujeres embarazadas (para evitar la exposición a los rayos X) o las jóvenes menores de 20 años, ya que en estas la probabilidad de tener cáncer de mama es mínima. La importancia de la mamografía radica en que la neoplasia puede ser bilateral (3% de los casos) y no necesariamente palpable en la otra mama; por lo tanto, ante la presencia de un nódulo, debe explorarse el tejido mamario completo. Vale destacar que la mamografía puede ser normal en presencia de un cáncer palpable (se estima que esto ocurre en el 2% de los casos). Por otro lado, la tasa de falsos negativos en las mujeres jóvenes es de un 10% a un 22%. Aun así, si la mamografía y la palpación sugieren benignidad, el error (falsos negativos) puede llegar al 4% (sensibilidad combinada del 96%); mientras que si la exploración clínica y la mamografía sugieren malignidad el error (falsos positivos) se estima en un 3,6% (especificidad combinada del 96,4%). Muchas veces la mamografía convencional genera dudas diagnósticas y debe recurrirse a imágenes radiológicas específicas para aclarar los hallazgos. La mamografía por compresión localizada se solicita cuando hay distorsión en la arquitectura o cuando se quiere estudiar una imagen en una determinada incidencia. Su utilidad es mayor en los casos de tumoraciones no calcificadas rodeadas por tejido fibroglandular, en las que no es posible distinguir si se trata de nódulos verdaderos o de imágenes resultantes de la superposición del tejido. Otra técnica, la mamografía con magnificación, permite realizar, mediante la ampliación, un estudio más detallado de las microcalcificaciones o de nódulos muy pequeños.
- Ecografía mamaria: este método complementario utiliza ultrasonido para evaluarlas estructuras mamarias. Su utilidad reside en que permite diferenciar si las estructuras nodulares son sólidas o quísticas, e identificar la presencia de anormalidades en una mama densa (por ejemplo, la mama de una mujer joven). La ecografía no distingue en forma exacta si un nódulo es benigno o maligno, pero es útil para definir si se trata de una tumoración líquida o sólida, para evaluar una lesión en la profundidad de la mama o cuando la paciente se niega a la biopsia. También puede aportar información cuando el examen es dudoso y la mamografía es normal y constituye un instrumento de guía que facilita la punción de lesiones no palpables. Hay que recordar que la ecografía es una técnica operador dependiente y que se necesitan equipos modernos con transductores adecuados para evaluar correctamente la mama. En la ecografía, las masas quísticas benignas se caracterizan porque sus bordes anterior y posterior están bien delineados, por la ausencia de ecos en su interior y la presencia de refuerzo posterior. En estos casos, este método diagnóstico tiene una precisión del 96% al 100%. En las tumoraciones sólidas, las características que definen benignidad son su hiperecogenicidad, la presencia de bordes netos y una relación diámetro longitudinal/diámetro anteroposterior mayor de 1,4.
- Biopsias: existen varias formas de obtener tejido mamario en forma ambulatoria (biopsias ambulatorias). Estas son:
-Aspiración con aguja fina: se trata de un método simple, seguro y poco costoso. Sin anestesia local, se inserta una aguja fina en la masa y se procede a aspirar el material que debe ser enviado para el examen citológico. En forma inmediata permite la distinción entre una masa sólida y una quística. Ante las masas profundas o difíciles de palpar se puede emplear una orientación ecográfica o estereotáxica para detectar el nódulo.
-Core needle biopsy: requiere de anestesia local. Se introduce una aguja que perfora el tejido y obtiene una muestra de la zona a estudiar. La ventaja radica en que, al tomar una muestra cilíndrica de tejido (y no un aspirado celular) permite, en algunos casos, determinar la presencia de receptores hormonales u otros factores pronósticos. La técnica es más traumática y la aguja se orienta en forma ecográfica o estereotáxica con verificación de que las muestras adecuadas han sido obtenidas. La sensibilidad se estima entre 88% y 98%, y la especificidad, entre 97% y 100%.
-Mammotome: es una técnica novedosa que toma la muestra de tejido mediante un sistema de punción con corte y aspiración, a partir de la cual se obtienen cilindros tisulares de mayor volumen. La utilidad de esta técnica, de reciente desarrollo en nuestro país, radica en que permite hacer marcación y biopsia de la lesión al mismo tiempo.
-Biopsia escisional: sigue siendo el test de referencia (goldstandard). Se hace cuando fracasaron las otras técnicas. Las lesiones profundas o no palpables pueden requerir marcación mamográfica previa. Muchos expertos, ante una masa dudosa con características mamográficas patológicas, realizan directamente una biopsia intraoperatoria. Durante esta, a través del proceso de congelación, efectúan en un solo paso la estadificación y el tratamiento.(16)
Manejo de la paciente con una masa mamaria
Las estructuras que pueden confundir con respecto a si la masa es o no de origen mamario son la unión condrocostal, una costilla prominente o el borde de la mama. Si una masa mamaria está presente, es crucial su evaluación mediante el “triple esquema”: examen clínico mamario, mamografía y punción, con o sin citología del material obtenido. Esta aproximación diagnóstica permite reducir el error diagnóstico al 1%. Si la masa palpable es quística y muestra características de benignidad bien definidas, se asume que se trata de un quiste mamario simple y no es necesario realizar ningún otro control específico más allá de los recomendados como parte del rastreo en la población general. Si la masa es quística pero sus características no están bien definidas ecográficamente o son sugestivas de malignidad, se recomienda realizar una aspiración con aguja fina. Cabe resaltar que, en muchos casos, cuando la tumoración es accesible y el médico está entrenado de forma adecuada, puede realizarse directamente la aspiración con aguja fina sin necesidad de hacer una ecografía previa, ya que los resultados de la aspiración son los más útiles para definir el diagnóstico. Característicamente, cuando el nódulo mamario dominante es un quiste benigno, en la aspiración se obtiene un líquido claro, la masa desaparece y queda como secuela un defecto temporario en el tejido mamario. En estos casos, si la mamografía es normal, no es indispensable efectuar la citología, pero se debe citar a la paciente a las cuatro o seis semanas para verificar que el quiste no haya recidivado. Cuando el material aspirado tiene sangre, la tumoración persiste luego de la punción, el quiste se reproduce rápidamente o persiste la densidad en la mamografía de control, debe asumirse que se trata de un carcinoma quístico y será necesario programar una biopsia ambulatoria para confirmar el diagnóstico. Si la tumoración es sólida, siempre debe obtenerse material para analizar su histología (aun cuando la mamografía sea normal). Esto puede realizarse mediante la aspiración con aguja fina, corre needle biopsy o Mammotome. En este caso, se debe consultar al especialista con el objeto de definir cuál será el procedimiento más apropiado para obtener la muestra. Si las técnicas mencionadas fracasan en la búsqueda de material, se deberá efectuar una biopsia escisional.(16)
Interconsulta con el especialista
Los criterios de derivación al especialista dependen en parte del grado de entrenamiento que tenga el médico de atención primaria en las diferentes técnicas complementarias de diagnóstico. Trataremos de puntualizar aquí algunos de ellos:
- Mamografías dudosas o francamente anormales.
- Nódulo mamario que a la punción es sólido, o nódulo quístico cuyo líquido obtenido por punción contiene material sanguinolento, o no desaparece completamente.
- Quiste recurrente o recidivado.
- Derrame hemático o serohemático por el pezón.
- Derrame por el pezón unilateral persistente.
- Retracción, distorsión o ulceración de la piel o complejo aéreo del pezón.
- Nodularidad asimétrica persistente luego de la menstruación.
- Mastitis no puerperal con tumor sólido subyacente o recidivante.
Evaluación radiológica
Las herramientas radiológicas más comunes para obtener imágenes del tejido mamario son la mamografía, la ecografía y la resonancia magnética.
La mamografía es la imagen de primera línea para mujeres mayores de 35 años que presentan una nueva masa mamaria. También es útil para la detección de mujeres asintomáticas que se ajustan a sus criterios de detección regionales. Este proceso implica la obtención de imágenes de rayos X en un plano craneocaudal y oblicuo medio lateral para garantizar la obtención de imágenes de todo el tejido mamario. La mamografía tiende a tener mayor especificidad y menor sensibilidad que la ecografía.(17) Puede tener resultados negativos en hasta el 15% de las pacientes con cáncer de mama.(18)
La ecografía es preferible a la mamografía, ya que el tejido mamario tiende a ser más denso y presenta una proporción mucho menor de tejido graso. Este tejido denso dificulta la precisión de la mamografía y dificulta la detección de microcalcificaciones.(17)
La resonancia magnética también puede ser útil para evaluar un bulto mamario nuevo. No se utiliza de forma rutinaria porque es más cara y tiene tiempos de espera más largos, pero muestra una alta sensibilidad para detectar y delinear masas mamarias. Es la modalidad preferida para pacientes con cirugía de aumento mamario previa, ya que los implantes mamarios pueden distorsionar el parénquima subyacente en la mamografía o la ecografía. También puede recomendarse para pacientes de alto riesgo, como aquellas con mutaciones BRCA subyacentes conocidas.(19)
BI-RADS 5ta edición
El Breast Imaging Reporting and Data System (BI-RADS) es un sistema desarrollado por el American College of Radiology (ACR) para estandarizar los informes de imágenes mamarias, mejorar la comunicación entre los radiólogos y los médicos remitentes, y proporcionar una herramienta de aseguramiento de la calidad. Desde su creación en los años 90, BI-RADS ha evolucionado para incluir no solo mamografía, sino también ecografía y resonancia magnética de mama.(20-21)
BI-RADS se compone de un léxico que describe características específicas de las imágenes, lo que ayuda a reducir la variabilidad en la interpretación de los hallazgos. Este léxico es fundamental para categorizar las lesiones mamarias en diferentes niveles de sospecha de malignidad, lo que a su vez guía las recomendaciones de manejo clínico.(20-22) Las categorías de BI-RADS van del 0 al 6, en las que cada número representa un nivel de sospecha y una recomendación de manejo específica. Por ejemplo, BI-RADS 1 indica un hallazgo negativo, mientras que BI-RADS 5 sugiere una alta sospecha de malignidad.(23-24)
BI-RADS 0: estudio insuficiente o incompleto.
BI-RADS 1: estudio normal.
BI-RADS 2: características benignas.
BI-RADS 3: probablemente benigno (<2% de riesgo de malignidad).
BI-RADS 4: características sospechosas (divididas en categorías 4a, 4b y 4c, según la probabilidad de malignidad).
BI-RADS 5: probablemente maligno (>95% de probabilidad de malignidad).
BI-RADS 6: maligno (maligno comprobado en biopsia de tejido).
El sistema BI-RADS incluye diferentes clasificaciones de masas según la modalidad de imagen. En la mamografía, para ser considerada una masa, la lesión debe ser visible en dos proyecciones diferentes, tener bordes externos convexos y ser más densa en el centro que en la periferia. En la ecografía, una masa requiere visualización en dos planos diferentes. Las masas se definen según su forma, margen y densidad. En términos de forma, una masa se puede categorizar como redonda, ovalada o irregular. Los márgenes circunscritos son más propensos a ser benignos, mientras que los márgenes micro lobulados, indistintos o espiculados son más propensos a ser malignos. El margen también puede aparecer oscurecido. La densidad de la masa se compara con los tejidos normales circundantes (mayor, igual o menor) o puede reflejar grasa dentro de la masa.
La quinta edición de BI-RADS ha mejorado la armonización de los términos del léxico a través de las modalidades de mamografía, ecografía y resonancia magnética, y ha introducido nuevos términos para reflejar los avances tecnológicos.(21) Además, se han consolidado los descriptores de calcificaciones en categorías benignas y sospechosas, eliminando la categoría de “preocupación intermedia”.(21)
BI-RADS también se utiliza como herramienta de evaluación de calidad en programas de detección de cáncer de mama, como se ha demostrado en el programa de detección de cáncer de mama en los Países Bajos, donde se ha utilizado para estratificar el riesgo y mejorar la uniformidad en la aplicación del léxico.(25)
Características radiológicas de nódulos mamarios
Mamografía
Forma:
- Redondeada u ovalada: las lesiones benignas suelen tener una forma redondeada u ovalada, lo que indica un crecimiento simétrico. Ejemplos comunes de lesiones benignas incluyen quistes y fibroadenomas.
- Irregular: las lesiones de forma irregular pueden indicar malignidad, ya que los tumores malignos tienden a crecer de manera asimétrica.(26)
Márgenes:
- Circunscritos: los márgenes bien definidos y lisos son típicos de lesiones benignas, ya que estas crecen de forma expansiva y no invaden el tejido circundante.
- Indistintos: márgenes mal definidos pueden indicar malignidad, especialmente si hay una transición difusa entre el nódulo y el tejido mamario adyacente.
- Espiculados: los márgenes espiculados son altamente sospechosos de malignidad, ya que sugieren la presencia de desmoplasia, una reacción fibrosa del estroma mamario que rodea a la lesión.(26)
Densidad:
- Densidad baja o grasa: las lesiones con baja densidad suelen ser benignas. Ejemplos incluyen lipomas o ganglios linfáticos intramamarios.
- Densidad intermedia o igual al tejido glandular: los fibroadenomas y otros nódulos benignos suelen presentar una densidad intermedia.
- Densidad alta: las lesiones malignas suelen ser de alta densidad en comparación con el tejido mamario circundante, debido a su contenido celular y estructural.
Calcificaciones:
- Las calcificaciones asociadas a un nódulo también son un factor importante. Las calcificaciones benignas suelen ser grandes, gruesas y dispersas. Las microcalcificaciones agrupadas o en patrones lineales o ramificados aumentan la sospecha de malignidad, ya que pueden estar asociadas a carcinomas ductales in situ.
Ecografía
Forma:
- Redondeada u ovalada: característica de lesiones benignas.
- Irregular: sugiere malignidad.
Márgenes:
- Circunscritos: típicos de nódulos benignos (como fibroadenomas).
- Mal definidos o espiculados: sugieren malignidad.
Ecogenicidad:
- Hipoecoico: nódulos benignos suelen ser hipoecoicos.
- Heterogéneo o complejo: puede indicar malignidad.
Otros signos:
- Refuerzo posterior: común en lesiones benignas.
- Sombra acústica: suele verse en nódulos malignos.
Resonancia magnética
Morfología:
- Lesiones redondeadas, ovaladas o lobuladas: suelen asociarse con nódulos benignos.
- Lesiones con contornos irregulares: se asocian más frecuentemente con malignidad.(26)
Márgenes:
- Circunscritos: característico de lesiones benignas.
- Irregulares o espiculados: característicos de nódulos malignos.
Patrón de realce:
- Homogéneo: suelen ser benignos.
- Heterogéneo o anular: sugiere malignidad.
Cinética del realce:
- Realce rápido con lavado temprano (tipo III): se asocia con mayor probabilidad de malignidad.
- Realce progresivo o tipo II: puede ser benigno, aunque algunos tumores malignos también muestran este patrón.(26)
Tratamiento
El tratamiento de un nódulo mamario nuevo depende de si el bulto es benigno o maligno y de la salud física y los deseos personales de la paciente. Cualquier paciente con una masa maligna comprobada o sospechada debe recibir un tratamiento con un enfoque interprofesional, con la participación de los equipos de oncología, radiología, patología, cirugía, enfermería especializada, anestesia, cuidados paliativos, trabajadores sociales y psicología cuando corresponda. Los cánceres de mama se tratan típicamente con cirugía, quimioterapia, radioterapia, terapia hormonal y terapia inmunológica.(27) Las masas mamarias benignas se tratan según la etiología:
- Quiste mamario: un quiste mamario simple suele involucionar sin ninguna intervención. Tiende a reaparecer si persiste o es problemático, pero puede ser una opción la aspiración del quiste. El aspirado del quiste puede enviarse para análisis citológico, pero existe cierta controversia en cuanto a los beneficios de esto debido al riesgo de falsos positivos.(28)
- Fibroadenoma: estas lesiones son benignas y generalmente involucionan sin tratamiento adicional. Se han introducido una amplia gama de indicaciones para intervenciones en fibroadenomas de mama, que incluyen crecimiento rápido, tamaño mayor a 3 cm, aumento en la categoría BI-RADS y diagnóstico de tejido sugestivo de hiperplasia atípica o sospecha de tumor filodes. A pesar del amplio uso del abordaje de escisión abierta para el manejo de fibroadenomas de mama, se ha utilizado la biopsia de mama asistida por vacío guiada por ecografía para la confirmación diagnóstica antes del manejo definitivo.(29) Sin embargo, si son grandes, dolorosos o causan malestar al paciente, se debe considerar la consulta quirúrgica y, a menudo, se eliminan quirúrgicamente.(30) Si hay incertidumbre sobre el diagnóstico, se debe realizar una biopsia por escisión con fines diagnósticos.
- La necrosis grasa y el hematoma no suelen requerir tratamiento, salvo analgésicos y control. Sin embargo, el cirujano especialista debe tener en cuenta si la masa está provocando al paciente un dolor importante o problemas estéticos.(31)
- Absceso mamario: en general, los abscesos requieren una incisión quirúrgica y drenaje para identificar y eliminar la fuente de infección. Los abscesos más pequeños, de menos de 3 cm de tamaño, y los abscesos de la lactancia pueden resolverse con antibióticos orales y aspiración con aguja, pero existe el riesgo de recurrencia.(32) En el contexto primario, los abscesos de la lactancia deben tratarse con analgesia y antibióticos orales. Se debe alentar a las pacientes a continuar amamantando y, si es posible, derivarlas para un tratamiento definitivo. El absceso en una paciente que no está amamantando o un absceso no resuelto, grande o multiloculado puede requerir la admisión para antibióticos intravenosos y drenaje quirúrgico o radiológico. En estos casos, se debe buscar la opinión temprana de un especialista en mama.(33) Los abscesos en una mujer que no está amamantando requieren la derivación a una clínica de triple evaluación para descartar un cáncer de mama inflamatorio subyacente(32)
- Ginecomastia: en los hombres que presentan ginecomastia, la investigación debe centrarse en la causa probable y, si no se encuentra ninguna, se recomienda una derivación a endocrinología.(34)
- Mastitis: se han introducido varias terapias antibióticas estándar, como el tratamiento estándar para la mastitis aguda. La elección del antibiótico a seleccionar para el tratamiento difiere considerando el microorganismo causal, el perfil de resistencia a los antibióticos y el historial positivo de mastitis recurrente. En consecuencia, la dicloxacilina-flucloxacilina, la cefalexina y la clindamicina son tratamientos estándar para la mastitis estafilocócica, la mastitis en pacientes con intolerancia a la penicilina y la mastitis recurrente, respectivamente. Los tratamientos mencionados deben ofrecerse durante una duración completa de 7 a 14 días.(35)
Pronóstico
Hay varios factores que deben tenerse en cuenta al interpretar el pronóstico de una masa mamaria. Entre ellos, los niveles de esteroides sexuales son significativamente importantes. Los esteroides sexuales endógenos son factores de riesgo bien establecidos para el cáncer de mama y dan lugar a una mayor tasa de crecimiento del tumor en mujeres posmenopáusicas. Además, los resultados de los niveles de hormonas esteroides en una mujer posmenopáusica con una masa mamaria podrían predecir el riesgo de desarrollar cáncer de mama en hasta 20 años. El riesgo de desarrollar cáncer de mama se correlaciona directamente con los niveles de hormonas sexuales circulantes, y los cinco determinantes principales de las hormonas sexuales esteroides circulantes son el alcohol, el ejercicio, la dieta, el peso corporal y el tabaquismo.(36-37)
Enfoque metodológico
Este estudio adoptó un diseño longitudinal, descriptivo y retrospectivo, en el que se incluyó un total de 181 pacientes, todas de sexo femenino, con edades a partir de los 18 años. Las pacientes asistieron al Hospital General de Agudos “José María Ramos Mejía” entre el 31 de octubre de 2022 y el 31 de octubre de 2024 para realizar estudios diagnósticos de ecografía mamaria. El trabajo se llevó a cabo bajo la categoría I de la OMS, cumpliendo con las normativas de la Ley Nacional (ANMAT) y la Guía de Buenas Prácticas Clínicas en Investigación en Salud, que no requieren consentimiento informado en este contexto.
La confidencialidad de los datos personales de las pacientes fue estrictamente resguardada según lo estipulado en la Ley 25.326, artículo 8°, referente al registro de datos y al secreto profesional.
De las 181 pacientes, solo 50 cumplieron con los criterios de inclusión y se procesaron sus muestras en el Servicio de Patología. Los resultados histopatológicos revelaron: 56% de lesiones benignas y 44% de lesiones malignas. Las ecografías fueron realizadas utilizando un equipo Vinno E10 y Phillips clearvue 550 (ver Anexos 1 y 2).
Para el procedimiento de toma de muestras se llevó a cabo la localización de las lesiones mediante guía ecográfica.
El procedimiento de toma de muestra incluyó los siguientes pasos:
- Preparación y asepsia:
-Organización de una mesa con materiales estériles.
-Realización de asepsia y antisepsia en la región a intervenir.
- Anestesia local:
-Infiltración por planos con lidocaína.
- Biopsia por punción:
-Introducción de una aguja de corte 14 Gauge bajo guía ultrasonográfica hasta la lesión identificada.
-Realización de múltiples disparos para obtener una cantidad adecuada de material para análisis.
- Posprocedimiento:
-Hemostasia local.
-Colocación de vendaje compresivo.
-Educación a la paciente sobre signos de alarma y recomendaciones posbiopsia.
No se registraron complicaciones inmediatas en las pacientes tras el procedimiento. Las muestras obtenidas fueron enviadas al Servicio de Histopatología del hospital para su análisis definitivo.
El diseño y la ejecución del estudio cumplieron con las normativas éticas y legales vigentes, protegiendo los derechos y la privacidad de las pacientes.
Este estudio refuerza la importancia del uso de guías clínicas y procedimientos estandarizados en el diagnóstico de nódulos mamarios visibles por ecografía.
Recopilación de datos
La recolección de datos para este estudio se llevó a cabo mediante un análisis exhaustivo de los registros disponibles en diferentes sistemas de gestión del hospital. Se utilizó la base de datos SIGEOS, que almacena información clínica, diagnóstica y de procedimientos realizados entre los años 2022 y 2024.
La búsqueda incluyó:
- Reportes de ecografías y biopsias ecodirigidas del Servicio de Imágenes Diagnósticas del Hospital General de Agudos “José María Ramos Mejía”.
- Resultados de exámenes histopatológicos obtenidos tanto de la base de datos del Servicio de Patología del hospital como del sistema SIGEOS.
- Datos imagenológicos gestionados a través del sistema SYNAPSE, utilizado para el almacenamiento y visualización de estudios radiológicos e informes diagnósticos.
Estos sistemas permitieron consolidar la información necesaria para el análisis retrospectivo, garantizando la integridad, confidencialidad y trazabilidad de los datos.
Criterios de inclusión
- Pacientes con nódulos mamarios clasificados como BI- RADS 4 por ecografía entre el período comprendido entre octubre de 2022 y octubre de 2024.
- Dicha ecografía que da el reporte BI-RADS 4 debió ser realizada en el Servicio de Imágenes Diagnósticas del Hospital Ramos Mejía.
- Las pacientes fueron sometidas a punción ecodirigidas en el Servicio de Imágenes Diagnósticas del Hospital Ramos Mejía.
Criterios de exclusión
- Pacientes con nódulos no visibles por ecografía.
- Pacientes con nódulos con clasificación BI-RADS diferente.
- Pacientes que no realizaron la punción en el Servicio de Imágenes Diagnósticas del Hospital Ramos Mejía o que el estudio histopatológico no fue realizado en el Servicio de Patología de dicho hospital.
Interpretación y análisis de resultados
- Análisis longitudinal descriptivo y retrospectivo.
- Utilización del sistema de archivo y transmisión de imágenes SYNAPSE.
- Lectura, interpretación y reporte de imágenes a cargo de médicos especialistas en diagnóstico por imágenes a través del sistema BI-RADS 4.
- Diseño y tabulación de los datos de pacientes por medio de Microsoft Excel para su posterior redacción por medio de Word.
- Recopilación de datos histológicos e inmunohistoquímicos realizada a través del laboratorio de planta, empleando marcadores específicos. Esta información fue complementada con los reportes proporcionados por el Servicio de Anatomía Patológica.
Resultados
En este estudio, se analizó un total de 181 pacientes con lesiones mamarias visibles por ecografía. De estas pacientes, 50 cumplieron con los criterios de inclusión. Todas las participantes fueron mujeres mayores de 18 años atendidas en el Hospital General de Agudos “José María Ramos Mejía” entre octubre de 2022 y octubre de 2024.
Dentro del análisis de resultados podemos describir lo siguiente:
Distribución general de lesiones encontradas
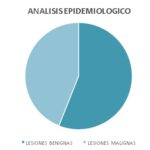
Gráfico 1
De los casos incluidos, el 56% correspondió a lesiones benignas (28 pacientes) y el 44% a lesiones malignas (22 pacientes), lo que resalta la relevancia de las biopsias ecodirigidas para discriminar entre estas entidades en pacientes con lesiones sospechosas (BI-RADS 4).
Distribución por porcentajes
Gráfico 2
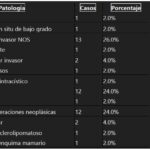
Las lesiones benignas más frecuentes fueron los fibroadenomas (24%), seguidos por casos clasificados como sin alteraciones neoplásicas (24%); luego tenemos las proliferaciones papilares con un 4%, y con un 2% encontramos las adenosis simples, mastitis crónica y tejido glandular esclerolipomatoso. Entre las lesiones malignas, el carcinoma ductal invasor de tipo no específico representó el mayor porcentaje (26%), seguido del carcinoma lobulillar invasor con un 4%, y por último, con un 2%, se presentaron carcinoma ductal in situ de bajo grado, carcinoma infiltrante, carcinoma mucinoso y carcinoma papilar intraquístico.
Media de edad por lesión
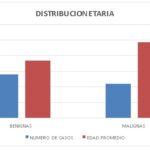
Gráfico 3
Se observó que las lesiones benignas predominaron en mujeres jóvenes, con una edad promedio de 36,8 años, mientras que las malignas fueron más comunes en pacientes mayores, con una edad promedio de 48,5 años.
Rango de edad por lesión
Gráfico 4
Dentro del rango etario se observó que las lesiones benignas se presentan entre los 25 y 49 años, mientras que la mayoría de las lesiones malignas se presentan entre los 40 y 62 años.
Sensibilidad – especificidad
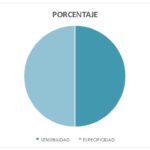
Gráfico 5
Con respecto a la sensibilidad, el 50% de los casos malignos fueron correctamente identificados, y haciendo referencia a la especificidad, el 50% de los casos benignos fueron correctamente identificados. Estos valores sugieren que el desempeño diagnóstico de las biopsias ecodirigidas para identificar lesiones malignas en pacientes con clasificación BI-RADS 4 es moderado. El sistema tiene una capacidad limitada tanto para detectar en forma correcta las lesiones malignas como para excluir de manera adecuada las benignas.
Discusión
Los resultados obtenidos en este estudio reflejan la relevancia y los desafíos del manejo diagnóstico de las lesiones mamarias sospechosas detectadas por ecografía. Se identificaron lesiones benignas en el 56% de los casos y malignas en el 44%, lo que subraya la importancia de las biopsias ecodirigidas en pacientes con lesiones sospechosas (BI-RADS 4), dado que aproximadamente la mitad de estas resultaron malignas. Según estudios previos, este enfoque es esencial para reducir procedimientos quirúrgicos innecesarios en lesiones benignas y garantizar un diagnóstico temprano en lesiones malignas. Los fibroadenomas y el carcinoma ductal invasor de tipo no específico fueron las lesiones más frecuentes dentro de las categorías benigna y maligna, respectivamente. Esto es consistente con reportes epidemiológicos previos que indican que los fibroadenomas son las neoplasias benignas más comunes en mujeres jóvenes, mientras que el carcinoma ductal invasor representa el subtipo maligno más prevalente.
Se observó que las lesiones benignas predominan en mujeres más jóvenes, con un promedio de 36,8 años, mientras que las malignas son más comunes en pacientes mayores, con un promedio de 48,5 años. Este patrón etario es congruente con la literatura, que asocia la mayoría de los tumores benignos con etapas tempranas de la vida reproductiva y un incremento en la incidencia de neoplasias malignas con la edad, debido a factores acumulativos, como la exposición hormonal y mutaciones genéticas somáticas.
La sensibilidad y especificidad del sistema utilizado para identificar lesiones malignas y benignas fueron del 50% cada una. Estos valores moderados indican que, aunque las biopsias ecodirigidas son útiles, su desempeño puede estar influenciado por factores, como la calidad del equipo de imagen, la experiencia del operador y las características histológicas de las lesiones. La sensibilidad relativamente baja podría derivar en falsos negativos, lo que podría retrasar el diagnóstico de lesiones malignas.
La mayoría de las lesiones benignas se encontraron en mujeres de entre 25 y 49 años, mientras que las malignas prevalecieron en el rango de 40 a 62 años. Este solapamiento de rangos destaca la necesidad de realizar evaluaciones exhaustivas en mujeres dentro de estas edades, especialmente en aquellas con factores de riesgo asociados.
En conjunto, estos hallazgos refuerzan la importancia de una aproximación diagnóstica integral para garantizar un manejo adecuado y oportuno de las lesiones mamarias sospechosas.
Conclusión
Las biopsias ecodirigidas representan una herramienta diagnóstica valiosa en el manejo de lesiones mamarias sospechosas, particularmente en pacientes clasificadas como BI-RADS 4. Sin embargo, su sensibilidad y especificidad moderadas limitan su capacidad para discriminar de manera óptima entre lesiones benignas y malignas, lo que sugiere la necesidad de continuar mejorando estas técnicas. La prevalencia de lesiones malignas en este estudio, que alcanza el 44%, destaca la importancia de un abordaje diagnóstico oportuno, dado el impacto significativo que el diagnóstico precoz tiene en el pronóstico y manejo de estas patologías.
El patrón etario identificado refuerza la necesidad de una vigilancia adecuada en mujeres jóvenes con lesiones benignas y un control más estricto en pacientes mayores, quienes presentan un mayor riesgo de desarrollar neoplasias malignas. Además, se observa la necesidad de optimizar los métodos diagnósticos mediante la incorporación de técnicas complementarias, como el uso de elastografía o análisis moleculares, para mejorar la precisión diagnóstica y reducir el margen de error en el manejo de lesiones mamarias sospechosas.
Recomendaciones
- Implementar capacitaciones continuas para los operadores y personal médico encargado de realizar las biopsias ecodirigidas.
- Incorporar tecnologías avanzadas, como la elastografía y la resonancia magnética con contraste, para complementar los hallazgos ecográficos en lesiones sospechosas.
- Establecer un protocolo claro basado en el riesgo, que considere la edad, antecedentes familiares y hallazgos imagenológicos, para determinar la necesidad de procedimientos adicionales o seguimiento estrecho.
- Dado el nivel de falsos negativos observado, se recomienda un seguimiento estricto de las pacientes con lesiones benignas clasificadas por biopsias, especialmente en aquellas con factores de riesgo adicionales.
- Realizar estudios adicionales que incluyan un mayor número de pacientes para validar los hallazgos y evaluar el impacto de nuevas tecnologías en la precisión diagnóstica.
Bibliografía
- Gossner, J. (2016). Albert Salomon (1883-1976): Pionier der Mammografie und Verfolgter des National sozialismus, Senologie, 13(04), 166-167. https://www.thieme–connect.com/products/ejournals/abstract/10.1055/s–0042119675
- Egan, R. L. (1960). Mammography. Thomas Publisher. https://books.google.com.ar/books/about/Mammography.html?id=VrhsAAA AMAAJ&redir_esc=y
- American College of Radiology (ACR). ACR BI-RADS® Atlas – Breast Imaging Reporting and Data System. https://www.acr.org/Clinical–Resources/Reporting–and–Data–Systems/BiRads
- Zhang, H., Qiu, L. and Peng, Y. (2018). The sonographic findings of micropapillary pattern in pure mucinous carcinoma of the breast, World Journal of Surgical Oncology, 16, 151. https://www.researchgate.net/publication/326599064_The_sonographic_findi ngs_of_micropapillary_pattern_in_pure_mucinous_carcinoma_of_the_breast
- Medina, D. (1976). Lesiones preneoplásicas en cáncer mamario murino. Cancer Res, 36(7 PT 2):2589-95. https://pubmed.ncbi.nlm.nih.gov/179706/
- Kisseberth, W. C., Sandgren, E. P. (2004). Desarrollo policlonal de nódulos preneoplásicos mamarios de ratón. Cancer Res, 64(3), 857-63. https://aacrjournals.org/cancerres/article/64/3/857/512169/PolyclonalDevelopment–of–Mouse–Mammary
- Harvey, S. C., Denison, C. M., Lester, S. C. et al. (1999). Nódulos fibrosos encontrados en una biopsia de mama con aguja gruesa: características de las imágenes. Radiology, 211(2), 535. https://pubs.rsna.org/doi/10.1148/radiology.211.2.r99ma42535?url_ver=Z39.88–2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
- Sanati, S., Leonard, M., Khamapirad, T., Eltorky, M. A. (2005). Mucinosis nodular de la mama: informe de un caso con hallazgos patológicos, ecográficos y clínicos y revisión de la literatura. Archives of Pathology & Laboratory Medicine, 129(3), e58-61. https://meridian.allenpress.com/aplm/article/129/3/e58/459151/NodularMucinosis–of–the–Breast–A–Case–Report–With
- Rodríguez, P. P., Crabtree, M., Venegas, R., Ozao-Choy, J., Dauphine, C. (2022). Adenoma del pezón: una enfermedad benigna de presentación sospechosa; 31348221117026. https://journals.sagepub.com/doi/full/10.1177/00031348221117026?rfr_dat=c r_pub++0pubmed&url_ver=Z39.88–2003&rfr_id=ori%3Arid%3Acrossref.org
- Siegel, R., Naishadham, D., Jemal, A. (2013). Estadísticas de cáncer. CA Cancer J Clin, enero, 63(1), 11-30. https://acsjournals.onlinelibrary.wiley.com/doi/10.3322/caac.21166
- Stachs, A., Stubert, J., Reimer, T., Hartmann, S. (2019). Enfermedad mamaria benigna en mujeres. Dtsch Arztebl Int., 116(33-34), 565-574. https://www.aerzteblatt.de/int/archive/article/209397
- Jan, M., Mattoo, J. A., Salroo, N. A., Ahangar, S. (2010). Triple evaluación en el diagnóstico de cáncer de mama en Cachemira. Indian J Surg, 72(2), 97-103. https://pmc.ncbi.nlm.nih.gov/articles/PMC3452506/
- Akram, M., Iqbal, M., Daniyal, M., Khan, A. U. (2017). Conciencia y conocimiento actual sobre el cáncer de mama. Biol Res, 50(1), 33. https://biolres.biomedcentral.com/articles/10.1186/s40659–017–0140–9
- Yalaza, M., İnan, A., Bozer, M. (2016). Cáncer de mama masculino. J Breast Health,12(1), 1-8. https://pmc.ncbi.nlm.nih.gov/articles/PMC5351429/
- Travis, R. C., Key, T. J. (2003). Exposición a estrógenos y riesgo de cáncer de mama. Breast Cancer Res, 5(5), 239-47. https://breast–cancer–research.biomedcentral.com/articles/10.1186/bcr628
- Dreyer, C., Discacciati, V., Bakalar, K., Spina, S. (2012). Nódulos mamarios y Mastalgia. Evid Act Pract Ambul, 15(4), 148-151. https://evidencia.org.ar/index.php/Evidencia/article/view/6163
- Tan, K. P., Mohamad Azlan, Z., Rumaisa, M. P., Siti Aisyah Murni, M. R., Radhika, S., Nurismah, M. I., Norlia, A., Zulfiqar, M. A. (2014). La precisión comparativa de la ecografía y la mamografía en la detección del cáncer de mama. Med J Malasia, 69(2), 79-85. https://pubmed.ncbi.nlm.nih.gov/25241817/
- Coveney, E. C., Geraghty, J. G., O’Laoide, R., Hourihane, J. B., O’Higgins, N. J. (1994). Razones que subyacen a una mamografía negativa en pacientes con cáncer de mama palpable. Clin Radiol, 49(2), 123-5. https://pubmed.ncbi.nlm.nih.gov/8124890/
- Wong, T., Lo, L. W., Fung, P. Y., Lai, H. Y., She, H. L., Ng, W. K., Kwok, K. M., Lee, C. M. (2016). Imágenes por resonancia magnética para el aumento de senos: una revisión gráfica. Insights Imaging, 7(3), 399-410. https://link.springer.com/article/10.1007/s13244–016–0482–9
- Eghtedari, M., Chong, A., Rakow-Penner, R., Ojeda-Fournier, H. (2021). Estado actual y futuro de BI–RADS en imágenes multimodales, de la serie especial sobre informes de radiología y sistemas de datos. American Journal of Roentgenology, 216(4), 860-873. https://www.ajronline.org/doi/10.2214/AJR.20.24894
- Rao, A. A., Feneis, J., Lalonde, C., Ojeda-Fournier, H. (2016). Una revisión ilustrada de los cambios en el BI–RADS quinta edición. RadioGraphics, 36(3), 623-39. https://pubs.rsna.org/doi/10.1148/rg.2016150178?url_ver=Z39.88–2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
- Burnside, E. S., Sickles, E. A., Bassett, L. W. et al. (2009). La experiencia del ACR BIRADS: aprendiendo de la historia. JACR, 6(12), 851-60. https://linkinghub.elsevier.com/retrieve/pii/S1546–1440(09)00390–1
- Balleyguier, C., Ayadi, S., Van Nguyen, K. et al. (2007). Clasificación BIRADS en Mamografía. European Journal of Radiology, 61(2), 192-4. https://linkinghub.elsevier.com/retrieve/pii/S0720–048X(06)00475–X
- Obenauer, S., Hermann, K. P., Grabbe, E. (2005). Aplicaciones y revisión de la literatura de la clasificación BI–RADS. Eu Radiol, 15(5), 1027-36. https://link.springer.com/article/10.1007/s00330–004–2593–9
- Timmers, J. M., van Doorne-Nagtegaal, H. J., Zonderland, H. M. et al. (2012). El sistema de información y datos de imágenes mamarias (BI–RADS) en el programa holandés de detección del cáncer de mama: su función como herramienta de evaluación y estratificación. Eu Radiol, 22(8), 1717-23. https://link.springer.com/article/10.1007/s00330–012–2409–2
- ACR BI-RADS® Atlas – Breast Imaging Reporting and Data System. American College of Radiology.
- Akram, M., Iqbal, M., Daniyal, M., Khan, A. U. (2017). Conciencia y conocimiento actual sobre el cáncer de mama. Biol Res, 50(1), 33. https://pubmed.ncbi.nlm.nih.gov/28969709/
- Berg, W. A., Sechtin, A. G., Marques, H., Zhang, Z. (2010). Masas mamarias quísticas y la experiencia con ACRIN 6666. Radiol Clin North Am, 48(5), 931-87. https://linkinghub.elsevier.com/retrieve/pii/S0033–8389(10)00088–6
- Peng, Y., Xie, F., Zhao, Y., Wang, S. (2021). Sociedad China de Cirugía de Mama. Guía de práctica clínica para fibroadenoma de mama: Guía de práctica de la Sociedad China de Cirugía de Mama (CSBrS). Chin Med J (Engl), 134(9), 1014-1016. https://journals.lww.com/cmj/fulltext/2021/05050/clinical_practice_guideline _for_breast.2.aspx
- Ajmal, M., Khan, M., Van Fossen, K. (2022). Fibroadenoma de mama. StatPearls Publishing; Treasure Island (FL). https://www.ncbi.nlm.nih.gov/books/NBK535345/
- Genova, R., Garza, R. F. (2023). Necrosis grasa mamaria. StatPearls Publishing; Treasure Island (FL). https://www.ncbi.nlm.nih.gov/books/NBK542191/
- Toomey, A. E., Le, J. K. (2023). Absceso mamario. StatPearls Publishing; Treasure Island (FL). https://pubmed.ncbi.nlm.nih.gov/29083702/
- Boakes, E., Woods, A., Johnson N, Kadoglou N. (2018). Infección mamaria: una revisión de las prácticas de diagnóstico y tratamiento. Eur J Breast Health, 14(3), 136-143. https://eurjbreasthealth.com/articles/doi/ejbh.2018.3871
- Johnson, R. E., Murad, M. H. (2009). Ginecomastia: fisiopatología, evaluación y tratamiento. Mayo Clin Proc, 84(11), 1010-5. https://linkinghub.elsevier.com/retrieve/pii/S0025–6196(11)60671–X
- Angelopoulou, A., Field, D., Ryan, C. A., Stanton, C., Hill, C., Ross, R. P. (2018). Microbiología y tratamiento de la mastitis humana. Med Microbiol Immunol, 207(2), 83-94. https://pubmed.ncbi.nlm.nih.gov/29350290/
- Folkerd, E., Dowsett, M. (2013). Hormonas sexuales y riesgo y pronóstico del cáncer de mama. Breast, 22 Suppl 2: S38-43. https://linkinghub.elsevier.com/retrieve/pii/S0960–9776(13)00142–2
- Cespedes Feliciano, E. M., Kwan, M. L., Kushi, L. H., Chen, W. Y., Weltzien, E. K., Castillo, A. L., Sweeney, C., Bernard, P. S., Caan, B. J. (2017). Índice de masa corporal, subtipo PAM50, recurrencia y supervivencia entre pacientes con cáncer de mama no metastásico. Cancer, 123(13), 2535-2542. https://acsjournals.onlinelibrary.wiley.com/doi/10.1002/cncr.30637