Autores: Nubia López, Julieth Salas, Joaquín Cueto, Heideman Castaño, Salomón Londoño
Resumen
La hidradenitis supurativa (HS) es una enfermedad dolorosa y crónica, que afecta en especial la unidad folículo-pilosebácea de la piel ubicada en ingle, axilas, región perianal, perineo, genitales y submamaria, regiones anatómicas donde se encuentran glándulas sudoríparas apocrinas. El curso clínico de la HS es heterogéneo, pues varía desde formas muy graves, con abscesos fluctuantes profundos y drenajes eventuales, con cicatrices residuales graves, hasta otra forma de enfermedad comparativamente leve, caracterizada por la aparición de algunos nódulos inflamatorios, pústulas y pápulas, de manera recidivante.
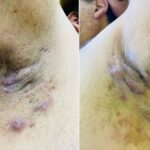
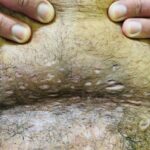
Se presenta el caso de un paciente masculino de 45 años, con antecedentes de obesidad mórbida, gangrena de Fournier (2012), hidradenitis supurativa de 15 años evolución, quien realizó múltiples tratamientos, fue tratado con adalimumab y antibióticos vía oral. Al examen físico presenta pápulas, pústulas, múltiples nódulos abiertos y cerrados localizados en cara, cuello, axilas, pliegues inguinales y perineales, con drenaje de material seropurulento, lesiones cicatrizales en las mismas zonas y úlceras en actividad en cara externa de ambas piernas. El diagnóstico de hidrosadenitis supurativa se realiza con la inclusión de estos tres criterios clínicos:
- Las lesiones se deben localizar en pliegues.
- Se deben observar las lesiones consideradas típicas (nódulos dolorosos, abscesos y cicatrices).
- Curse de forma recurrente o crónica. Para el diagnóstico de esta patología no se deben realizar más pruebas complementarias. Solo se debe realizar biopsia o cultivo cuando haya dudas diagnósticas o complicaciones de las lesiones.
El tratamiento de primera línea se realizó con antibioterapia sistémica con rifampicina y clindamicina; resorcinol tópico, una crema queratolítica y antiséptica, y la aplicación de un corticoide tópico. Además de tratamiento médico se le indican unas medidas para evitar el empeoramiento o recidiva de las lesiones, como el abandono del tabaco, no vestir ropa ajustada y evitar el sobrepeso. A los tres meses el paciente acude a revisión, donde se encuentra mejoría clínica, consiguiendo remisión completa de las lesiones.
Palabras clave: hidradenitis supurativa, adalimumab, enfermedades autoinflamatorias, folículos pilosos, apocrinitis.
Introducción
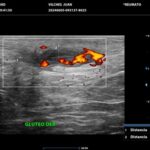
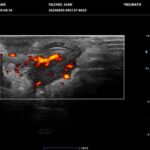
La HS es una enfermedad crónica, inflamatoria inmunomediada, sistémica, recurrente y debilitante de los folículos pilosos terminales con origen en las glándulas apocrinas de estos. Presenta habitualmente lesiones dolorosas, profundas e inflamadas, localizadas más frecuentemente en las regiones axilares, inguinales y anogenitales. El 80% de las lesiones tienen ubicación profunda de difícil acceso al examen físico. Su diagnóstico es clínico pero el ultrasonido (US) de alta resolución con Doppler es un método que cumple actualmente un rol esencial para establecer el diagnóstico, estadificar la enfermedad y detectar actividad, incluso en el caso de lesiones no pesquisadas en el examen físico. También nos permite monitorear el estado y la progresión de la HS, facilitando la evaluación rápida de distintos enfoques terapéuticos. Incluso, los cambios ecográficos pueden modificar la conducta terapéutica.
Hallazgos imagenológicos
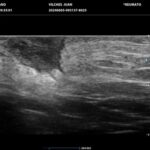
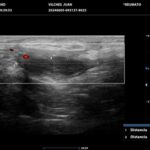
Los hallazgos ecográficos más relevantes son el ensanchamiento de folículos pilosos, engrosamiento y ecogenicidad anormal de la dermis, nódulos pseudoquísticos dérmicos, colecciones líquidas y tractos fistulosos. Por otro lado, el US nos permite valorar la localización exacta y extensión de las lesiones, su ecogenicidad, el grado de vascularización al examen Doppler y las eventuales complicaciones, e incluso la modificación de las lesiones en respuesta a la terapéutica instaurada. La HS se estadifica clínicamente mediante la clasificación de Hurley y los hallazgos ecográficos muestran correlación con cada estadio clínico.
Discusión
La HS es una patología inflamatoria crónica, que se presenta con nódulos dolorosos, comedones gigantes y trayectos fistulosos, una de las sinonimias más utilizadas es “acné inverso”. Además, es una enfermedad recurrente, que cursa con un importante impacto en la calidad de vida de los pacientes. Afecta a todas las etnias, con una prevalencia mundial estimada del 1%, según los estudios europeos. Presenta cierto predominio en climas tropicales y calurosos, pero se reportan casos desde lugares del mundo con condiciones climáticas variables. En Argentina no se conoce la incidencia exacta en la población general. La HS es más frecuente en mujeres. La incidencia en el sexo femenino es mayor entre los 20 y los 40 años, la relación se invierte luego de los 45 años. Desde de los 55 años se observa una disminución significativa de la prevalencia en ambos sexos. La HS se puede iniciar en la pubertad y, entre un 2% y un 3%, antes de los 11 años.
La HS es una enfermedad inflamatoria multifactorial. El folículo piloso cumple un papel primordial en el desarrollo de la enfermedad, demostrado por la presencia de tapones de queratina como fenómeno inicial y la inflamación de la glándula apocrina como evento secundario. La hiperplasia epidérmica, con la obstrucción del folículo, provoca la dilatación de este, consecuentemente la aparición de los primeros eventos inflamatorios. Luego se produce la rotura folicular con derrame de su contenido (bacterias, sebo, queratina, fragmentos pilosos) a la dermis, lo que da inicio a un proceso inflamatorio tardío con formación de nódulos, abscesos y posterior aparición de tractos fistulosos.
El factor genético se ha demostrado en un porcentaje inferior al 50% de los casos, vinculándose su presencia a un peor pronóstico. Los genes responsabilizados están en el cromosoma 1p211.1- 1q25.3.7. Se ha localizado una mutación en la vía de señalización Notch de la enzima γ-secretasa, se ha descrito la inactivación del gen ncstn, ubicado en 1q22-23 que codifica la nicastrina, una de las subunidades de la γ-secretasa y proteasa. Además, en una familia con formas clínicas graves, se han encontrado dos mutaciones en subunidades génicas relacionadas con la γ-secretasa del potenciador de presilina I y II (psen1 y psenen). Se ha considerado cierta relación entre la HS y la enfermedad de Crohn por mutua vinculación con el gen card15.
Aun no se conoce con exactitud la función del microbioma bacteriano, ni la de la biopelícula que recubre las fístulas. Esto podría relacionarse con el inicio de la enfermedad o con su continuación. En el futuro es probable que, además de antibioterapia específica, se intente modificar el microbioma bacteriano, en lugar de erradicarlo, mediante trasplante de flora y utilización de péptidos antimicrobianos sintéticos.
Otros factores predisponentes o desencadenantes son el tabaco, la obesidad, factores endocrinológicos, ropa ajustada, desodorantes o depilación, ya que los irritantes exacerban enfermedad y, por último, algunos fármacos como el litio, los anticonceptivos o la isotretinoína son algunos de los medicamentos que pueden generar brotes repetitivos de la enfermedad. (Hidradenitis supurativa: reporte de un caso, Lacerda MS1 y col).
Si bien no es lo más frecuente, se han comunicado casos de HS en niños. Estos pacientes suelen tener antecedentes de hipotiroidismo congénito, hiperplasia suprarrenal, obesidad o pubertad precoz, por lo que es recomendable realizar un examen endocrinológico para descartarlos.
Se describen enfermedades que se vinculan con la HS, que se conocen como comorbilidad. Entre estas se encuentran el desarrollo de artritis HLA B27 negativa y la Enfermedad Inflamatoria Intestinal (EII), especialmente en el caso de enfermedad de Crohn (EC); ambas son patologías inflamatorias crónicas que con mayor frecuencia se vinculan con la HS. Como dijimos antes, se ha observado cierta relación entre la HS y el síndrome metabólico (SM). Estos resultados se describieron tanto en la población adulta como en la pediátrica. Existe también una relación proporcional entre el SM y la gravedad de la HS. Además, se ha demostrado una mayor presencia de depresión y ansiedad, en pacientes con HS que en la población sana.
El diagnóstico es clínico y ecográfico. No hay una prueba específica para el diagnóstico ni marcadores de laboratorio específicos. Un estudio ha demostrado que la mayoría de los pacientes (80%) experimentan uno o más síntomas prodrómicos. Estos son: fatiga, malestar general, cefalea y náuseas. Los síntomas localizados incluyeron eritema, parestesia y prurito. Estos pueden aparecer entre las 12 y las 24 horas previas a las manifestaciones clínicas. Posteriormente aparecen nódulos no inflamatorios (sin eritema y con baja sensibilidad) e inflamatorios (con eritema y dolor), que pueden resolverse de manera espontánea al cabo de siete a 15 días o progresar a abscesos, fístulas o cicatrices. Las localizaciones más frecuentes según el sexo, son las siguientes:
-Mujeres: zona genital e inguinal (93%), zona axilar (67%), pliegue interglúteo (33%), glúteos (23%), región submamaria y aréola (22%).
-Hombres: zona axilar (79%), genital (77%), pliegue interglúteo (51%), glúteos (40%) y región submamaria (5%).
Existen localizaciones inusuales, como: nuca, región retroauricular, cintura abdominal, conducto auditivo externo, párpados y ombligo.
El diagnóstico ecográfico resulta de importancia diagnóstica, tal es así que la ecografía de alta resolución y el estudio Doppler han ocupado un lugar preponderante en los últimos años. La ecografía de la piel permite identificar lesiones no encontradas en el examen físico, evaluando de manera fehaciente su extensión anatómica. El empleo de la ecografía en la HS es ideal, ya que el 80% de las lesiones ocurren en las capas más profundas y no en la superficie de la piel. Permite evaluar la localización exacta y extensión de las lesiones, su ecogenicidad, el grado de vascularización al examen Doppler, las eventuales complicaciones, e incluso la respuesta terapéutica.
Respecto de los diagnósticos diferenciales, en las etapas iniciales la HS debe distinguirse del acné, ántrax, forúnculos, quiste dermoide, erisipela, quistes epidermoides, abscesos peri-rectales y quistes pilonidales. En la etapa tardía, las enfermedades a diferenciar son actinomicosis, fístulas anales, enfermedad de Crohn, enfermedad por arañazo de gato, granuloma inguinal, linfogranuloma venéreo, nocardiosis, TBC, tularemia, pioderma gangrenoso, entre otros. Para la clinimetría se emplean diferentes escalas, como la Hurley, Sartorius, entre otras. Estas permiten clasificar la HS según su gravedad y además objetivar su evolución clínica y la respuesta terapéutica. Sin embargo, el método de Hurley no es adecuado para evaluar la respuesta terapéutica, ya que este es estático, no cuantitativo y no tiene en cuenta la actividad inflamatoria, aunque es útil para decidir una eventual intervención quirúrgica. A pesar de todo, en Argentina se exige como estándar para la prescripción terapéutica. El estadio I se corresponde con HS leve, consistente en abscesos únicos o múltiples sin cicatrices ni fistulas. Los estadios II y III se corresponden con las formas moderadas y graves; el estadio II se caracteriza por la presencia de uno o más abscesos recurrentes con formación de fistulas y cicatrices y el estadio III, por iguales lesiones, pero que afectan toda una región anatómica.
El método de Hurley modificado es una nueva clasificación que incluye la evaluación de la presencia de trayectos fistulosos, el grado de inflamación y la extensión, le permite al médico evaluar la gravedad en los diferentes fenotipos de HS y ayuda a adecuar el tratamiento. Este método reconoce que los pacientes clasificados como Hurley I-II originales pueden ser considerados dentro de estadios graves, además se redefine Hurley III como pacientes con afectación del 1% de la superficie corporal y tractos fistulosos inflamatorios intercomunicados. Estas modificaciones ayudan en el momento de elegir la opción terapéutica más adecuada, sea esta terapia antiinflamatoria, cirugía, o terapias biológicas, incluso permite considerar graves a pacientes Hurley I, siendo también útiles para reconocer cuando la cirugía no es conveniente.
Conclusión
El estudio ecográfico de alta resolución con Doppler tiene un rol fundamental en la categorización de las lesiones de HS en profundidad, incluso las subclínicas. Debemos incluir al US como técnica de elección para estadificar y monitorear pacientes con HS, ya que nos permite acceder a un diagnóstico rápido de lesiones típicas con las que podremos, en conjunto con la clínica, estadificar y seguir en el tiempo a los pacientes.
Bibliografía
García-Martínez, F. J., Pascual, J. C., López-Martín I., Pereyra-Rodríguez, J. J., Martorell Calatayud, A., Salgado-Boquete, L. et al. (2017). Actualización en hidrosadenitis supurativa en Atención Primaria. SEMERGEN – Medicina de Familia, (43)1, 34-42.
González, C. P. (2020). Hidradenitis supurativa. Descripción de los hallazgos ecográficos en un centro de referencia en Bogotá, Colombia. Rev. Asoc Colomb Dermatol, 28(3), 240-249. DOI: https://doi.org/10.29176/2590843X.1533
Lacerda, M. S., Bau, M. N. (2023). Hidradenitis supurativa: reporte de un caso. Rev. argent. dermatol, 104 [citado 2024-08-26], 21-30. http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S1851-300X2023000100021&lng=es&nrm=iso>. ISSN 1851-300X
Landeras Álvaro, R. M., Gallardo Agromayor, E. C., Lamagrande Oregon, A., De Diego Diez, A., Pozo Piñón, F., González López, M. A. (2018). Valoración ecográfica de la Hidradenitis supurativa. Lo que el dermatólogo necesita saber. Seram, 2(1). https://piper.espacio-seram.com/index.php/seram/article/view/8362
Scala, E., Cacciapuoti, S., Garzorz-Stark, N., Megna, M., Marasca, C., Seiringer, P., Volz, T., Eyerich, K. Fabbrocini, G. (2021). Hidradenitis Suppurativa: Where We Are and Where We Are Going. Cells, Aug 15, 10(8), 2094. doi: 10.3390/cells10082094. PMID: 34440863; PMCID: PMC8392140.