Autor: Fausto Simeon Mestra Cervantes
Tutor del TFI: Dr. Andrés Vanrell
Directora de la carrera: Dra. Marta Kura
Resumen
La sarcoidosis pulmonar es una enfermedad inflamatoria de causa desconocida que se caracteriza por la formación de granulomas en los pulmones y otros órganos. Este estudio analizó la epidemiología, diagnóstico y tratamiento de la sarcoidosis pulmonar en el Hospital Tornú durante los últimos diez años, con el objetivo de comprender mejor sus características y mejorar su manejo clínico. Los resultados mostraron una mayor prevalencia de la sarcoidosis en mujeres (86,7%) y en adultos jóvenes, con un pico de incidencia entre los 31 y 40 años. Se observó que los síntomas más comunes son tos y disnea, mientras que los métodos diagnósticos principales incluyeron radiografías de tórax y tomografías computarizadas (TCAR). El tratamiento más comúnmente utilizado fueron los corticoides, con inmunosupresores reservados para casos más graves. El estudio subrayó la importancia de un enfoque individualizado en el diagnóstico y tratamiento, así como la necesidad de más investigaciones multicéntricas y prospectivas para fortalecer el conocimiento sobre la sarcoidosis pulmonar. Las recomendaciones incluyeron promover la concientización entre los profesionales de la salud y establecer protocolos estandarizados para el manejo de la enfermedad.
Palabras clave: sarcoidosis pulmonar, diagnóstico, Hospital Tornú, radiografías de tórax, tomografías computarizadas (TCAR).
Introducción
La sarcoidosis pulmonar fue reconocida como una enfermedad granulomatosa sistémica de etiología desconocida, que afectó principalmente a los pulmones y a los ganglios linfáticos hiliares. Su diagnóstico y seguimiento clínico representaron un desafío constante debido a la variabilidad de sus manifestaciones radiológicas, lo que resaltó la importancia de las técnicas de imagen en su manejo. A lo largo de los años, se produjeron avances significativos en las herramientas de imagen utilizadas para la detección y monitorización de esta patología, desde la radiografía convencional hasta técnicas más avanzadas, como la tomografía computarizada (TC), la resonancia magnética (RM) y la tomografía por emisión de positrones (PET).
A pesar de los avances en el campo de la radiología, persistió una brecha en la comparación sistemática de las técnicas de imagen a través de los diferentes estadios de la sarcoidosis pulmonar y su efectividad en la evaluación de la progresión y respuesta al tratamiento. Esta situación generó la necesidad de realizar un análisis exhaustivo que permitiera determinar cuáles de estas técnicas ofrecían los mayores beneficios diagnósticos y pronósticos. Además, la variabilidad en los hallazgos radiológicos y la falta de criterios estándar complicaron la identificación temprana de la sarcoidosis y su correcta clasificación.
Este estudio resultó relevante dado que la sarcoidosis pulmonar presentó una evolución heterogénea y el diagnóstico temprano pudo mejorar de manera significativa el pronóstico de los pacientes. Al analizar retrospectivamente la efectividad de las distintas técnicas de imagen utilizadas en el Hospital de Agudos Dr. Enrique Tornú, este trabajo no solo buscó llenar el vacío en la literatura sobre el uso comparativo de estas técnicas, sino también contribuir a la optimización de los protocolos de diagnóstico y seguimiento en estos pacientes.
El presente análisis se llevó a cabo en el Hospital de Agudos Dr. Enrique Tornú, una institución de referencia en el tratamiento de enfermedades respiratorias en la ciudad de Buenos Aires, donde se atendió un alto volumen de pacientes con sarcoidosis pulmonar. El estudio abarcó un período de diez años, durante el cual se empleó un enfoque retrospectivo para recolectar y analizar los datos obtenidos de los estudios de imagen de los pacientes diagnosticados con esta enfermedad. La comparación entre técnicas de imagen incluyó la radiografía de tórax, la tomografía computarizada, el PET y la resonancia magnética, con el fin de evaluar su efectividad en la detección, clasificación y seguimiento de los casos.
Los resultados de este estudio permitieron comprender mejor la utilidad de las distintas técnicas de imagen en el diagnóstico y manejo de la sarcoidosis pulmonar, contribuyendo así al desarrollo de guías clínicas más precisas para su uso en la práctica médica. Además, proporcionaron información valiosa para mejorar la planificación del tratamiento y la evaluación de la respuesta terapéutica de los pacientes, optimizando así el cuidado que se les brindó.
Diagnóstico
La sarcoidosis pulmonar había sido reconocida como una enfermedad granulomatosa crónica que podía tener un curso progresivo, convirtiéndose en una causa importante de morbilidad, en especial en poblaciones susceptibles.1 Dado que el diagnóstico oportuno y la monitorización adecuada eran esenciales para el manejo efectivo de la enfermedad, se volvió imperativo estudiar cómo las técnicas de imagen contribuían a estos procesos. Este análisis retrospectivo se justificó por la necesidad de optimizar las herramientas diagnósticas en un entorno clínico real, como el hospital de agudos Dr. Enrique Tornú, que poseía una larga trayectoria en el manejo de enfermedades respiratorias.
Además, este trabajo buscó identificar características radiológicas clave para la detección temprana de la sarcoidosis, lo que podría tener implicaciones significativas en el pronóstico y tratamiento de los pacientes.2 La evaluación de las diferentes técnicas de imagen permitiría establecer un protocolo más efectivo para el diagnóstico y seguimiento de esta enfermedad.3
La presentación clínica de la sarcoidosis era variable, y el diagnóstico podía resultar desafiante debido a la naturaleza multisistémica de la enfermedad. A pesar de que su etiología seguía siendo desconocida, se creía que tanto factores genéticos como ambientales jugaban un papel en su patogénesis.
En los años anteriores, las técnicas de imagen habían evolucionado de modo significativo, mejorando la precisión en el diagnóstico y seguimiento de la sarcoidosis. Las radiografías de tórax, la tomografía computarizada (TC), la resonancia magnética (RM) y la tomografía por emisión de positrones (PET) demostraron ser herramientas valiosas para evaluar la extensión de la enfermedad y monitorear la respuesta al tratamiento.4 Sin embargo, existía incertidumbre sobre la capacidad de estas técnicas para identificar con precisión los estadios iniciales de la enfermedad o predecir su evolución, lo que limitaba su uso optimizado en la práctica clínica diaria.
Ante este panorama, el estudio retrospectivo se inició con el objetivo de llenar esas lagunas de conocimiento. Al mirar hacia atrás, los profesionales del hospital Dr. Enrique Tornú identificaron la necesidad de analizar y comparar de manera sistemática las diferentes modalidades de imagen utilizadas en los últimos diez años, con el fin de determinar cuáles ofrecían mejores resultados en términos de diagnóstico temprano, evaluación de la progresión y monitorización de la respuesta al tratamiento. Esta revisión se perfilaba como un paso clave hacia la optimización de las prácticas de diagnóstico y tratamiento de la sarcoidosis pulmonar, con la esperanza de impactar de manera positiva en los pronósticos de los pacientes afectados y mejorar su calidad de vida.
Radiografía de tórax
Las radiografías de tórax anormales son comunes en pacientes con sarcoidosis, presentándose en más del 90% de los casos. Se observa linfadenopatía hiliar bilateral en 50%-80% de los pacientes y opacidades pulmonares parenquimatosas en 25%-60% de los casos. Para la estadificación de la enfermedad pulmonar se utiliza el sistema de puntuación radiográfica Scadding, que se basa en la presencia de adenopatías y opacidades pulmonares.
- La enfermedad en estadio I se caracteriza por la presencia de adenopatías hiliares y mediastínicas bilaterales, con una alta probabilidad de remisión radiográfica y sintomática.
- En el estadio II se observan opacidades pulmonares no fibróticas junto con linfadenopatía hiliar y mediastínica, y también hay una alta probabilidad de remisión espontánea.
- En el estadio III se presentan anomalías parenquimatosas no fibróticas sin adenopatías, y la regresión espontánea es menos común.
- El estadio IV se caracteriza por cambios fibróticos en la radiografía de tórax, con menor probabilidad de regresión espontánea.
Sin embargo, el sistema de estadificación Scadding ha sido criticado por su falta de correlación con la gravedad de la enfermedad y su limitada utilidad pronóstica. En cambio, la tomografía computarizada (TC) se considera más sensible para detectar anomalías en el parénquima pulmonar y ha reemplazado en gran medida a la radiografía convencional en el diagnóstico de la sarcoidosis.
Tomografía computada
La exploración por tomografía computarizada (TC), que se utilizó por primera vez diez años después de que se describiera el sistema de estadificación Scadding, ha reemplazado desde entonces a la CXR convencional y ha demostrado ser mucho más sensible que la radiografía de tórax para representar anomalías del parénquima pulmonar en pacientes con sarcoidosis.
Aunque las TC son ampliamente utilizadas en pacientes con sarcoidosis, su papel en el seguimiento, el pronóstico y la orientación terapéutica aún no está bien establecido. Se recomienda considerar la TC cuando existan hallazgos clínicos o radiográficos atípicos, sospecha de complicaciones o condiciones superpuestas, sospecha clínica de sarcoidosis con radiografía de tórax normal, o en pacientes candidatos a trasplante pulmonar. La TCAR es preferible debido a su mayor capacidad para detectar anomalías sutiles y distinguir entre fibrosis e inflamación en diferentes estadios de la enfermedad.
Hallazgos en la TCAR en la sarcoidosis
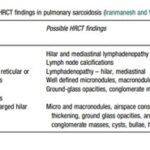
La sarcoidosis pulmonar se caracteriza por varios hallazgos en la tomografía computarizada de alta resolución (TCAR). Estos incluyen linfadenopatía hiliar y paratraqueal bilateral bien definida, opacidades nodulares y micronodulares con distribución perilinfática. Los nódulos son redondeados y suelen tener un tamaño de 2 a 4 mm. También se observa el agrandamiento y calcificación de los ganglios linfáticos hiliares bilaterales. Las calcificaciones pueden presentar diferentes aspectos, como amorfo, puntiforme (parecido a una palomita de maíz) o similar a una cáscara de huevo. La distribución perilinfática de las lesiones micronodulares es el patrón parenquimatoso más frecuente. Con el tiempo, estas lesiones pueden fusionarse y formar macronódulos y conglomerados similares a masas, con la presencia de pequeños nódulos satélites alrededor de las masas conglomeradas, lo que se conoce como “signo de galaxia”.
En la TCAR se pueden encontrar otros hallazgos menos frecuentes, como cambios fibróticos con opacidades lineales y bronquiectasias por tracción, opacidades parcheadas en vidrio esmerilado, consolidación parcheada del espacio aéreo (alveolitis sarcoide o sarcoidosis alveolar), opacidades reticulares lineales aisladas, halo inverso o signo del atolón. La sarcoidosis pulmonar también muestra un patrón de atenuación en mosaico debido a la afectación granulomatosa o fibrosis de las vías respiratorias pequeñas, lo cual puede estar asociado con obstrucción en las pruebas de función pulmonar. El atrapamiento de aire es común pero no específico de la sarcoidosis y puede estar presente en cualquier etapa radiográfica de la enfermedad. Se detectan anomalías traqueobronquiales en la TC, con engrosamiento y estenosis de la pared bronquial, que se correlacionan con los hallazgos broncoscópicos.
La estenosis bronquial puede ser causada por acumulación de granulomas endobronquiales, compresión extrínseca de las vías respiratorias debido a ganglios linfáticos agrandados en el mediastino, o distorsión de los bronquios debido a enfermedad parenquimatosa fibrótica en etapa terminal. El bronquio del lóbulo medio derecho es el más afectado en la sarcoidosis. En casos avanzados y de alto riesgo, la TCAR puede mostrar quistes fibróticos, ampollas y enfisema paracicatricial, que indican una etapa avanzada de la sarcoidosis. Estas lesiones tienden a afectar las zonas pulmonares superiores y medias, siguiendo las vías respiratorias más grandes en una distribución perihiliar. Los cambios quísticos subpleurales en panal se encuentran principalmente en las zonas pulmonares superiores y medias, mientras que las bases pulmonares se ven menos afectadas. Se debe considerar la fibrosis pulmonar idiopática en el diagnóstico diferencial cuando las bases pulmonares están involucradas.
Los cambios quísticos subpleurales en panal también pueden estar presentes en la sarcoidosis fibrótica, pero en general se localizan en las zonas pulmonares superiores y medias, mientras que las bases pulmonares se ven menos afectadas. Es importante considerar la fibrosis pulmonar idiopática (FPI) en el diagnóstico diferencial cuando las bases pulmonares están involucradas, ya que ambas enfermedades pueden coexistir en algunos pacientes. La presencia de aspergilomas y otras bolas fúngicas (micetomas) es una complicación temida en pacientes con sarcoidosis fibroquística. Estas bolas de hongos se desarrollan en ampollas y quistes preexistentes y pueden causar infección secundaria o provocar hemoptisis potencialmente mortal. La coexistencia de sarcoidosis y aspergiloma pulmonar conlleva un alto riesgo de muerte.
Marco teórico
Sarcoidosis pulmonar
La sarcoidosis pulmonar es una enfermedad multisistémica que impacta profundamente la calidad de vida de quienes la padecen. Se caracteriza por la formación de granulomas no caseificantes, que son pequeñas acumulaciones de células inflamatorias, y tiene su mayor incidencia en los pulmones. La prevalencia en Europa varía entre 10 y 40 casos por cada 100.000 habitantes. Esta cifra, aunque pueda parecer baja, representa un reto significativo en términos de diagnóstico y tratamiento, ya que la sarcoidosis se manifiesta de maneras muy diversas.5
Una de las características más desafiantes de la sarcoidosis es su capacidad para camuflarse. En sus etapas iniciales, los síntomas pueden ser sutiles o confundirse con otras condiciones respiratorias, lo que complica su identificación. Los pacientes a menudo experimentan tos seca, disnea y, en algunos casos, dolor torácico. Este espectro de síntomas puede llevar a un diagnóstico erróneo o retrasado, lo que subraya la importancia de un enfoque meticuloso y multidisciplinario para su evaluación.
La enfermedad es más común en personas jóvenes, específicamente entre los 20 y 40 años, y afecta de manera desproporcionada a las mujeres.6 Este patrón sugiere que la sarcoidosis podría estar relacionada con factores hormonales o ambientales que son más prevalentes en este grupo demográfico. Sin embargo, la etiología exacta de la enfermedad continúa siendo un misterio. Aunque se ha propuesto que factores genéticos y ambientales juegan un papel importante, la falta de consenso en la comunidad médica dificulta la creación de estrategias de prevención y tratamiento efectivas.
El diagnóstico de la sarcoidosis es un proceso intrincado que requiere un enfoque de exclusión. Los médicos deben combinar hallazgos clínicos, estudios de imagen y análisis anatomopatológicos para llegar a un diagnóstico certero.7 Esta metodología no solo exige un conocimiento profundo por parte del profesional de la salud, sino que también puede ser angustiante para los pacientes, quienes pueden sentir incertidumbre sobre su condición durante un tiempo prolongado.
En resumen, la sarcoidosis pulmonar es una enfermedad que representa tanto un desafío clínico como humano. Su diagnóstico complejo y la variabilidad de sus síntomas resaltan la necesidad de una atención médica cuidadosa y personalizada. Comprender su naturaleza y las experiencias de quienes la padecen es fundamental para avanzar en su tratamiento y mejorar la calidad de vida de los pacientes. Este tema es de vital importancia no solo desde una perspectiva médica, sino también desde el punto de vista del bienestar integral del individuo.
La sarcoidosis es una enfermedad inflamatoria multisistémica que se caracteriza por la formación de granulomas no caseificantes en diversos órganos del cuerpo, siendo los pulmones y los ganglios linfáticos mediastínicos los más afectados. Esta condición puede involucrar prácticamente cualquier órgano, pero se observa con mayor frecuencia en los pulmones, la piel, los ojos y el hígado.
Aunque la causa exacta de la sarcoidosis aún es incierta, se cree que es el resultado de una respuesta inmunitaria alterada frente a un desencadenante ambiental o infeccioso en individuos genéticamente predispuestos.8
Papel de la ECA en la sarcoidosis
Producción en los granulomas
La enzima convertidora de angiotensina (ECA) juega un papel importante en la fisiopatología de la sarcoidosis, ya que se produce en grandes cantidades dentro de los granulomas que caracterizan a esta enfermedad. Los granulomas, que son formaciones de células inmunológicas, como macrófagos y linfocitos T, se encuentran principalmente en los pulmones y en los ganglios linfáticos. En estos granulomas, la ECA se sintetiza como parte de la respuesta inflamatoria. Se cree que esta enzima contribuye a la regulación del sistema renina-angiotensina, que está involucrado en la respuesta inmunitaria y en la regulación de la presión arterial.9, 10
Marcador de actividad de la enfermedad
La medición de los niveles de ECA en suero es un indicador ampliamente utilizado para monitorizar la actividad de la sarcoidosis. En muchos pacientes, los niveles de ECA tienden a estar elevados en relación con la actividad de la enfermedad, en especial en aquellos con afectación pulmonar y ganglionar (Nunes et al., 2015).
Sin embargo, la ECA no es específica de la sarcoidosis, ya que también puede encontrarse elevada en otras enfermedades granulomatosas y en procesos inflamatorios no granulomatosos.11
Limitaciones del diagnóstico
A pesar de su utilidad, el uso de la ECA como herramienta diagnóstica presenta ciertas limitaciones. No todos los pacientes con sarcoidosis muestran niveles elevados de ECA, y su medición puede no correlacionarse directamente con la gravedad de la enfermedad. De hecho, estudios han mostrado que hasta un 40% de los pacientes puede tener niveles normales de ECA, incluso en presencia de una enfermedad activa.12 Esto resalta la necesidad de utilizar la medición de ECA junto con otras pruebas y criterios clínicos para llegar a un diagnóstico definitivo.
Sensibilidad y especificidad
La sensibilidad y especificidad de la medición de ECA en sarcoidosis varían según los estudios, pero por lo general se encuentran en torno al 60%-70% para la detección de la enfermedad. Esta variabilidad depende de diversos factores, como la fase de la enfermedad, la localización de los granulomas y las condiciones clínicas del paciente. Además, factores individuales como la raza, el sexo y la presencia de otras comorbilidades pueden influir en los niveles de ECA, lo que limita su valor como prueba diagnóstica única.13
Utilidad clínica
El dosaje de ECA se emplea sobre todo como herramienta complementaria en el manejo de la sarcoidosis, no como una prueba de diagnóstico definitiva. Su principal utilidad radica en su capacidad para monitorear la actividad de la enfermedad durante el seguimiento de los pacientes. Los niveles elevados de ECA pueden sugerir que la enfermedad está activa, lo que puede guiar a los médicos en la evaluación de la respuesta al tratamiento. Sin embargo, su interpretación debe hacerse con cautela, considerando la posibilidad de falsos positivos y negativos, y en el contexto de la historia clínica del paciente.
Evaluación de la respuesta al tratamiento
Durante el tratamiento de la sarcoidosis, la medición periódica de los niveles de ECA puede ser útil para evaluar la respuesta al tratamiento. Una disminución de los niveles de ECA podría indicar una respuesta favorable a la terapia, mientras que una persistencia o aumento de los niveles podría sugerir que la enfermedad continúa siendo activa o que el tratamiento no es suficientemente eficaz. No obstante, su rol en la predicción de recidivas aún es un tema de debate, dado que no siempre se correlaciona con la progresión clínica de la enfermedad.14
En resumen, la enzima convertidora de angiotensina (ECA) desempeña un papel crucial en la fisiopatología de la sarcoidosis, siendo un marcador útil para monitorizar la actividad de la enfermedad. No obstante, su utilidad diagnóstica es limitada debido a su falta de especificidad y la variabilidad en sus niveles entre los pacientes. Por lo tanto, el dosaje de ECA debe considerarse una herramienta complementaria, utilizada en conjunto con otros hallazgos clínicos y pruebas diagnósticas para guiar el tratamiento y el seguimiento de los pacientes con sarcoidosis.
Técnicas de imagen en la evaluación de la sarcoidosis pulmonar
Radiografía de tórax
La radiografía de tórax se establece como una de las pruebas de imagen más utilizadas en la detección inicial de la sarcoidosis pulmonar. Su importancia radica en la capacidad de identificar adenopatías hiliares bilaterales, un hallazgo característico en los estadios iniciales de la enfermedad (estadios 0-i).15 Esta técnica permite clasificar la sarcoidosis en cinco estadios, que van desde la normalidad hasta la fibrosis pulmonar. Esta clasificación es fundamental, ya que no solo ayuda a los médicos a comprender la progresión de la enfermedad, sino que también proporciona un marco de referencia para determinar las opciones de tratamiento.
A pesar de su utilidad, la radiografía presenta limitaciones notables. Su capacidad para detectar lesiones pequeñas o sutiles es limitada, lo que puede resultar en diagnósticos erróneos o tardíos. Sin embargo, a pesar de estas restricciones, la radiografía sigue siendo una herramienta esencial en el manejo clínico, dado que permite un primer acercamiento a la patología, guiando las decisiones posteriores sobre el diagnóstico y tratamiento.16
Tomografía computarizada (TC)
La tomografía computarizada de alta resolución ha transformado el enfoque diagnóstico de la sarcoidosis pulmonar, aportando una precisión considerable en la identificación de características que no son visibles en una radiografía convencional. Estudios realizados por el autor destacan que la TC es especialmente efectiva para detectar micronódulos, cambios fibróticos y opacidades parenquimatosas, lo que resulta crucial en la diferenciación de la sarcoidosis de otras condiciones pulmonares, como la tuberculosis. Este tipo de imagen puede revelar manifestaciones atípicas, como las opacidades en “vidrio esmerilado” y los quistes subpleurales, que son indicativos de la sarcoidosis en lugar de otras enfermedades respiratorias.17
El análisis de la TC es vital no solo para el diagnóstico, sino también para el seguimiento de la progresión de la enfermedad. Permite a los médicos evaluar cómo avanza la sarcoidosis y ajustar el tratamiento en consecuencia, lo que puede mejorar significativamente la calidad de vida del paciente.
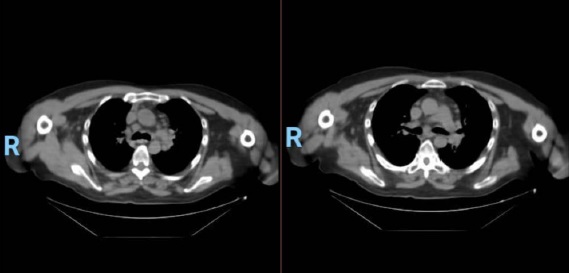
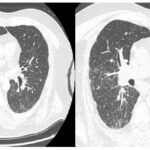
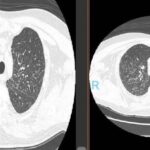
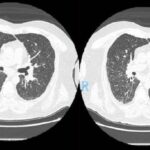
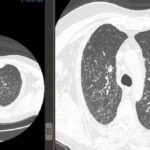
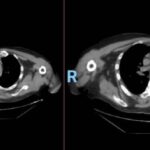
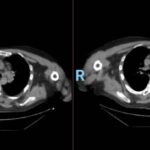
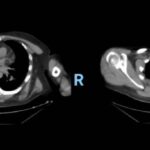
En la tomografía computada de tórax en ventana pulmonar se identifica un patrón micronodular con distribución perilinfática y difusa en ambos hemitórax. Este hallazgo se acompaña de un engrosamiento peribronquial notable, así como de opacidades en vidrio deslustrado, que predominan en las zonas subpleurales y en las regiones posteriores de ambos pulmones.
En la tomografía computada de tórax en ventana mediastínica se observan múltiples adenopatías localizadas en diversas áreas del cuello y mediastino. Estas adenopatías se distribuyen en las cadenas yúgulo-carotídeas, en ambas regiones supraclaviculares y a lo largo del mediastino, abarcando específicamente las siguientes áreas: la región paratraqueal superior derecha, los espacios retrocavo-pretraqueal y prevascular, la zona subcarinal, la ventana aortopulmonar y en la región de la arteria mamaria (AM). La presencia de estas adenopatías sugiere un compromiso linfático difuso en estas zonas.
Resonancia magnética (RM) y tomografía por emisión de positrones (PET)
La resonancia magnética (RM) y la tomografía por emisión de positrones (PET) desempeñan un papel fundamental en la evaluación de la sarcoidosis, en particular en la identificación de afectación extratorácica y en la monitorización de la actividad inflamatoria de la enfermedad.
La PET en especial ha demostrado ser una herramienta valiosa para detectar infecciones activas no solo en el tejido pulmonar, sino también en otros órganos. Esto es crucial para evaluar la respuesta al tratamiento, sobre todo en pacientes que reciben corticoides, ya que permite determinar si la inflamación ha disminuido o si se necesita ajustar el enfoque terapéutico.18
Ambas técnicas ofrecen información complementaria que puede ser decisiva en el manejo clínico de la sarcoidosis. La RM puede proporcionar detalles adicionales sobre la extensión de la enfermedad en los tejidos blandos, mientras que la PET ayuda a clarificar la actividad metabólica de las lesiones, lo que es esencial para una toma de decisiones informada sobre el tratamiento.
En conjunto, las diversas técnicas de imagen desempeñan un papel crítico en la evaluación y el manejo de la sarcoidosis pulmonar. Desde la radiografía de tórax, que sirve como primera línea de diagnóstico, hasta la TC y las técnicas más avanzadas como la RM y la PET, cada modalidad contribuye a un entendimiento más completo de la enfermedad. A medida que la tecnología avanza, se espera que la precisión en la detección y el seguimiento de la sarcoidosis continúe mejorando, ofreciendo esperanza a los pacientes afectados por esta compleja enfermedad.
Hallazgos radiológicos clave para el diagnóstico temprano
La sarcoidosis es una enfermedad multisistémica que afecta principalmente a los pulmones en más del 90% de los casos. Desde el punto de vista del diagnóstico por imágenes, los pacientes son clasificados en cuatro estadios radiológicos según la afectación pulmonar, basada en la clasificación de Scadding.19
- Estadio I: afectación de los ganglios linfáticos hiliares y mediastínicos sin compromiso pulmonar evidente.
- Estadio II: afectación ganglionar junto con opacidades pulmonares.
- Estadio III: afectación pulmonar sin compromiso ganglionar.
- Estadio IV: fibrosis pulmonar avanzada.
Las técnicas de imagen juegan un papel crucial no solo en la identificación de estos estadios, sino también en la monitorización de la respuesta al tratamiento y la progresión de la enfermedad. Las características clave en la TC incluyen la presencia de nódulos, opacidades en vidrio esmerilado y fibrosis pulmonar, mientras que en la PET se buscan áreas con mayor captación de 18f-fdg, lo que indica actividad inflamatoria.20, 21
La identificación temprana de la sarcoidosis pulmonar es fundamental para mejorar el pronóstico de los pacientes. Entre los hallazgos radiológicos más significativos se encuentran las adenopatías hiliares bilaterales, que suelen ser uno de los primeros signos detectables en las imágenes de tomografía computarizada (TC). Estos ganglios linfáticos agrandados son indicativos de los estadios iniciales de la enfermedad, específicamente en las fases I y II,22 destacan que este hallazgo es crítico, ya que la detección temprana puede facilitar intervenciones más efectivas y oportunas.
Además de las adenopatías, la distribución de micronódulos submilimétricos de manera perilinfática también es característica de la sarcoidosis. Estos pequeños nódulos pueden ser sutiles y difíciles de identificar, pero su presencia es un marcador clave en la evaluación diagnóstica. La correcta interpretación de estos hallazgos puede marcar una diferencia en el manejo clínico, ayudando a los médicos a diferenciar la sarcoidosis de otras condiciones respiratorias que pueden presentar síntomas similares.
A medida que la enfermedad avanza, los cambios radiológicos se vuelven más evidentes. La aparición de cambios fibróticos y opacidades en “vidrio esmerilado” son indicativos de una progresión hacia estadios más avanzados de la enfermedad. Estos hallazgos no solo son importantes desde el punto de vista diagnóstico, sino que también tienen implicaciones significativas para el pronóstico del paciente. La fibrosis pulmonar, una complicación grave, puede afectar la función respiratoria y la calidad de vida a largo plazo. Por lo tanto, la identificación de estos cambios es crucial para ajustar el tratamiento y planificar un seguimiento adecuado.23
Los hallazgos radiológicos, como las adenopatías hiliares y los micronódulos submilimétricos, juegan un papel vital en el diagnóstico temprano de la sarcoidosis pulmonar. Además, el reconocimiento de cambios fibróticos y opacidades avanzadas permite a los médicos no solo establecer un diagnóstico preciso, sino también prever posibles complicaciones, lo que es esencial para ofrecer un tratamiento eficaz y personalizado a los pacientes.
Uso de las técnicas de imagen en el seguimiento de la sarcoidosis
El seguimiento de la respuesta al tratamiento en la sarcoidosis pulmonar es fundamental para personalizar las estrategias terapéuticas y asegurar la mejor atención posible para los pacientes. Esta enfermedad, que puede tener un curso variable y a menudo impredecible, requiere una monitorización constante para ajustar el tratamiento según la evolución del paciente. En particular, los pacientes que reciben terapia con corticoides necesitan una evaluación regular para determinar la efectividad de la intervención y detectar cualquier efecto secundario o complicación.
Las investigaciones recientes han demostrado que la tomografía por emisión de positrones (PET) es especialmente eficaz para monitorear la inflamación residual en los tejidos pulmonares. Incluso en pacientes cuyos síntomas clínicos han mostrado mejoría, la PET puede revelar la presencia de inflamación persistente. Este hallazgo es crucial, ya que indica que, aunque un paciente pueda sentirse mejor, la enfermedad podría seguir activa en su interior, lo que podría requerir un ajuste en el tratamiento.24 Esto resalta la importancia no solo de confiar en la percepción de los síntomas, sino en herramientas diagnósticas avanzadas para tener un panorama completo del estado del paciente.
Además de la PET, la utilización continua de la tomografía computarizada (TC) es vital para evaluar la progresión de la sarcoidosis. La TC permite detectar cambios en la estructura pulmonar, lo que es en especial relevante en aquellos pacientes que desarrollan complicaciones como fibrosis o hipertensión pulmonares. Estos hallazgos radiológicos son clave para los médicos, ya que pueden ayudar a determinar si es necesario intensificar el tratamiento o, en algunos casos, considerar la posibilidad de una remisión. Esta capacidad de adaptar el enfoque terapéutico según los cambios observados en las imágenes es esencial para garantizar que los pacientes reciban la atención adecuada en cada etapa de su enfermedad.25
Las técnicas de imagen, como la PET y la TC, son herramientas invaluables en el seguimiento de la sarcoidosis pulmonar. Estas tecnologías no solo ayudan a monitorear la respuesta al tratamiento, sino que también permiten una comprensión más profunda de la evolución de la enfermedad. Al integrar estos hallazgos en la práctica clínica, los médicos pueden ofrecer un tratamiento más efectivo y adaptado a las necesidades individuales de sus pacientes, lo que puede marcar una diferencia significativa en su calidad de vida.
Antecedentes
Históricamente, la radiografía de tórax ha sido la técnica de imagen más utilizada para el diagnóstico inicial de la sarcoidosis pulmonar. La clasificación tradicional de Scadding se basa en hallazgos radiológicos y ha sido una herramienta útil para establecer el estadio de la enfermedad.26 Sin embargo, la tomografía computarizada (TC) ha demostrado ser más sensible para detectar cambios parenquimatosos y la afectación ganglionar, proporcionando una mejor evaluación de la extensión de la enfermedad.27
Por otro lado, la tomografía por emisión de positrones (PET) se ha utilizado para evaluar la actividad metabólica de los granulomas, lo que la convierte en una herramienta útil para determinar la actividad de la enfermedad y la respuesta al tratamiento.28 En cuanto a la resonancia magnética (RM), aunque su uso en sarcoidosis pulmonar es limitado, ha mostrado utilidad en la evaluación de la afectación extrapulmonar, como en el sistema nervioso central o en el corazón.29
La investigación titulada “Uso de Técnicas de Imagen en el Diagnóstico y Seguimiento de la Sarcoidosis Pulmonar” tuvo como objetivo revisar los casos clínicos de pacientes con sarcoidosis pulmonar, centrándose en los hallazgos radiológicos característicos, como adenopatías hiliares bilaterales y micronódulos perilinfáticos observados en tomografía computarizada (TC) y radiografías de tórax. La investigación concluyó que las técnicas de imagen, en especial la TC de alta resolución, son esenciales no solo para clasificar y monitorear la enfermedad, sino también para guiar las decisiones terapéuticas. Se enfatizó en la importancia de un diagnóstico temprano, que puede mejorar de manera significativa la calidad de vida de los pacientes y evitar complicaciones a largo plazo. Además, el estudio sugirió que la capacitación continua de los profesionales de la salud en la interpretación de imágenes es crucial para optimizar el manejo de la sarcoidosis pulmonar. Este trabajo revisó casos clínicos de pacientes con sarcoidosis pulmonar, centrándose en hallazgos radiológicos como adenopatías hiliares bilaterales y micronódulos perilinfáticos en TC y radiografías de tórax. La conclusión destaca la importancia de la TC de alta resolución para clasificar y monitorear la enfermedad.30
La tesis proporciona un marco sólido sobre la identificación de los hallazgos radiológicos característicos que son fundamentales para el diagnóstico temprano de la sarcoidosis. Al relacionar esto con las variables de estudio, se puede argumentar que la detección temprana mediante técnicas de imagen influye directamente en la progresión de la enfermedad y en la calidad de vida del paciente. El enfoque en la TC de alta resolución también sugiere que la tecnología de imagen avanzada es esencial para diferenciar la sarcoidosis de otras patologías pulmonares, una variable clave en la investigación que busca establecer un diagnóstico preciso.
La investigación titulada “Eficacia de técnicas de imagen en la identificación de Sarcoidosis pulmonar” tuvo como objetivo analizar la eficacia de diferentes técnicas de imagen, incluyendo la radiografía y la TC, en la identificación de sarcoidosis pulmonar en una cohorte de pacientes. Los hallazgos indicaron que la TC ofrecía una sensibilidad significativamente mayor en comparación con la radiografía, en especial en la detección de lesiones submilimétricas y cambios fibróticos. El estudio también propuso un protocolo de imagen para el diagnóstico y seguimiento de la enfermedad, resaltando la necesidad de personalizar el enfoque según la progresión de la sarcoidosis en cada paciente. Analizó la eficacia de la radiografía y la TC en la identificación de sarcoidosis pulmonar, encontrando que la TC ofrecía una sensibilidad mayor. También propuso un protocolo de imagen para el diagnóstico y seguimiento.31
La comparación entre radiografía y TC resalta la variable de la precisión diagnóstica en el seguimiento de la sarcoidosis. La mayor sensibilidad de la TC no solo subraya la importancia de seleccionar la técnica adecuada para cada paciente, sino que también implica un potencial impacto en la gestión de la enfermedad. La propuesta de un protocolo de imagen puede ser un aspecto valioso para estandarizar la atención, permitiendo una mejor comparación de resultados y una mayor coherencia en el manejo clínico de los pacientes. Esto se alinea con el tema de estudio al buscar un enfoque basado en la evidencia que respalde decisiones clínicas efectivas.
La tesis titulada “El papel de la PET en el Seguimiento de Pacientes con Sarcoidosis Pulmonar” tuvo como objetivo identificar la importancia que tiene el papel de la tomografía por emisión de positrones (PET) en el seguimiento de pacientes con sarcoidosis pulmonar. Los autores encontraron que la PET es en particular útil para evaluar la actividad inflamatoria residual, incluso en pacientes cuyas manifestaciones clínicas han mejorado. Este estudio sugirió que integrar la PET en el seguimiento podría ofrecer una mejor comprensión de la evolución de la enfermedad y ayudar en la toma de decisiones sobre el tratamiento, especialmente en pacientes con respuesta clínica parcial. Este trabajo se enfocó en el uso de la tomografía por emisión de positrones para evaluar la actividad inflamatoria residual en pacientes con sarcoidosis pulmonar, incluso cuando los síntomas clínicos habían mejorado.32
La utilización de la PET introduce una dimensión adicional al seguimiento de la sarcoidosis, enfatizando la variable de la actividad inflamatoria en contraste con la mejoría clínica. Este estudio resalta la importancia no solo de considerar los síntomas visibles, sino también la actividad patológica subyacente. La capacidad de la PET para identificar inflamación residual es crucial para ajustar el tratamiento y evitar posibles recaídas, un aspecto que puede influir directamente en el pronóstico del paciente. Este hallazgo se relaciona estrechamente con el tema de investigación, que busca entender cómo las técnicas de imagen no solo diagnostican, sino que también monitorean y guían el tratamiento de la sarcoidosis.
Estas investigaciones evidencian cómo las técnicas de imagen, como la TC y la PET, desempeñan un papel esencial en el diagnóstico y seguimiento de la sarcoidosis pulmonar. Cada estudio aporta perspectivas únicas sobre la precisión diagnóstica, la identificación de complicaciones y la adaptación del tratamiento, todas variables críticas que deben ser consideradas al desarrollar un enfoque integral para el manejo de esta compleja enfermedad. Integrar estos hallazgos en el marco de estudio fortalecerá la base teórica y práctica de la investigación, permitiendo una mejor comprensión de la influencia de las técnicas de imagen en el manejo de la sarcoidosis pulmonar.
Objetivos
Objetivo general
Evaluar la efectividad de las técnicas de imagen (radiografía de tórax, tomografía computarizada, PET, resonancia magnética) en la detección, clasificación y seguimiento de la sarcoidosis pulmonar en el Hospital de Agudos Dr. Enrique Tornú durante los últimos diez años.
Objetivos específicos
- Comparar las técnicas de imagen utilizadas en los diferentes estadios de la enfermedad.
- Identificar características radiológicas clave que permitan un diagnóstico temprano o una evaluación precisa de la progresión.
- Evaluar el papel de las imágenes en la monitorización de la respuesta al tratamiento.
Enfoque metodológico
Este estudio tuvo un carácter retrospectivo, basado en la revisión de expedientes clínicos de pacientes diagnosticados con sarcoidosis pulmonar en el Hospital de Agudos Dr. Enrique Tornú durante los últimos diez años. Los estudios retrospectivos se han utilizado ampliamente en investigaciones clínicas, ya que permitieron evaluar un volumen considerable de datos obtenidos de manera previa en contextos clínicos reales, proporcionando información valiosa para el análisis de la eficacia de intervenciones diagnósticas o terapéuticas.33, 34
Para cada paciente, se seleccionaron los estudios de imagen realizados, que incluyeron radiografías de tórax, tomografías computarizadas (TC), tomografías por emisión de positrones (PET) y resonancias magnéticas (RM).
La inclusión de varias modalidades de imagen permitió comparar su efectividad en diferentes fases de la enfermedad, como se había observado en estudios previos de enfermedades pulmonares granulomatosas, donde se constató que la TC era más precisa para detectar la extensión de la enfermedad en comparación con la radiografía de tórax.35, 36 Los casos fueron clasificados de acuerdo con los estadios de la enfermedad definidos por la clasificación de Scadding, una metodología clásica en la evaluación radiológica de la sarcoidosis pulmonar.37
Para cada modalidad de imagen se evaluaron las características clave, como la afectación de los ganglios linfáticos hiliares y mediastínicos, la presencia de opacidades pulmonares, la fibrosis y otras alteraciones pulmonares. Estudios previos han demostrado la importancia de estos hallazgos en la determinación del estadio y pronóstico de la enfermedad.38, 39
La investigación se llevó a cabo en el Servicio de Neumonología y Anatomía Patológica del Hospital de Agudos Dr. Enrique Tornú, situado en Combatientes de Malvinas 3002, entre Ávalos y Campillo, en la localidad de Villa Ortuzar, CABA.
El universo de la investigación estuvo compuesto por pacientes diagnosticados con sarcoidosis pulmonar que acudieron al Servicio de Neumonología del Hospital Dr. Enrique Tornú en los últimos diez años, sumando un total de quince pacientes.
Criterios de inclusión
- Adultos de ambos sexos, mayores de 20 años, que presentaron signos y síntomas sugerentes de la enfermedad.
- Pacientes que fueron diagnosticados y tratados en el Hospital Tornú durante el período de estudio de diez años.
- Pacientes con informes médicos completos y disponibles para revisión.
Criterios de exclusión
- Menores de 20 años.
- Pacientes con enfermedades infecciosas activas.
- Pacientes con diagnóstico exclusivo de sarcoidosis extrapulmonar (enfocándose específicamente en la sarcoidosis pulmonar).
- Pacientes con diagnóstico de otras enfermedades pulmonares crónicas, como enfermedad pulmonar obstructiva crónica (EPOC) o fibrosis pulmonar idiopática, que pudieran confundir los resultados o el análisis de los datos.
Unidad de observación
La unidad de observación correspondió a cada paciente adulto, sin distinción de sexo, mayor de 20 años, que presentó signos y síntomas sugestivos de la enfermedad y cumplió con los criterios de inclusión. Estos pacientes fueron considerados como unidades individuales de observación para la recopilación de datos registrados en las historias clínicas sobre sus características demográficas, manifestaciones clínicas, métodos diagnósticos y tratamientos utilizados. Los pacientes que no cumplieron con los criterios de inclusión o que fueron excluidos según los criterios establecidos no fueron considerados en esta unidad de observación.
Métodos y técnicas para la recolección de datos
- Se utilizó el método científico.
- Técnica: la técnica empleada para la recolección de información incluyó:
–Recopilación de datos: se obtuvo acceso a las historias clínicas y registros de anatomía patológica de los pacientes diagnosticados con sarcoidosis pulmonar en el Hospital Tornú durante el período de estudio.
–Revisión de literatura: se realizó una revisión exhaustiva de la literatura científica existente sobre la sarcoidosis pulmonar para respaldar los resultados y discusiones.
- Instrumento: se utilizó una hoja de recolección de datos.
Procedimientos para la recolección de datos
Inicialmente, se obtuvo el permiso de las autoridades pertinentes, incluyendo a la jefa de la División del Servicio de Anatomía Patológica, la División de Neumonología y la jefa del departamento de archivo del Hospital de Agudos Dr. Enrique Tornú. El estudio se llevó a cabo dentro de una estrategia de recolección de datos a partir de las historias clínicas de los pacientes diagnosticados con sarcoidosis y atendidos en el Hospital Tornú. Estos registros proporcionaron la información necesaria para la investigación.
En una primera etapa, se solicitó la obtención de los resultados de los informes de anatomía patológica compatibles con granulomatosis. Luego, se procedió a la búsqueda de las historias clínicas de los pacientes correspondientes, con el fin de recopilar datos demográficos y diagnósticos relevantes. Durante este proceso se excluyeron aquellos pacientes que no cumplían con los criterios de inclusión establecidos. Los datos de los pacientes seleccionados fueron registrados en una ficha de recolección de datos, y a partir de ellos se llevó a cabo el análisis necesario para establecer la incidencia de la sarcoidosis en el presente estudio.
Plan de tabulación y análisis
Se utilizó Microsoft Excel para la realización de gráficos y Microsoft Word para el análisis de los resultados.
Diseño del proceso
En el estudio sobre la sarcoidosis pulmonar el diseño del proceso incluyó una revisión exhaustiva de la literatura científica para identificar los métodos diagnósticos más efectivos. La planificación del proceso involucró la elección de técnicas de imagen específicas para la recolección de datos, destacando el uso de tomografías computarizadas de alta resolución (TCAR), las cuales demostraron ser significativamente más sensibles en la detección de alteraciones parenquimatosas.40 Este enfoque permitió no solo obtener imágenes más precisas, sino también facilitar una clasificación más detallada de los pacientes y un seguimiento del progreso de la enfermedad a lo largo del tiempo.
Los investigadores seleccionaron los instrumentos diagnósticos en función de su capacidad para correlacionar hallazgos radiológicos con manifestaciones clínicas. Inicialmente, se utilizó la puntuación Scadding para la estadificación de la enfermedad. Sin embargo, se puede optar por la TCAR en fases avanzadas debido a su mayor sensibilidad y especificidad en la evaluación de fibrosis pulmonar.41 Esto fue crucial, ya que el diagnóstico oportuno y preciso de la sarcoidosis pulmonar tiene implicaciones directas en el tratamiento y la calidad de vida del paciente.
La planificación del proceso también contempló la validación de los instrumentos mediante estudios previos. La recolección sistemática de datos utilizando protocolos estandarizados permite obtener conclusiones robustas sobre la progresión de las lesiones pulmonares en la sarcoidosis.42 Este enfoque no solo garantiza la validez de los datos, sino que también facilita la comparación con investigaciones anteriores, asegurando así que los hallazgos sean relevantes y aplicables a la práctica clínica.
Además, se consideraron las diferentes características demográficas de los pacientes, como la edad, el sexo y los antecedentes médicos, para asegurar que los resultados fueran representativos de la población afectada por sarcoidosis. Esto se alinea con las recomendaciones de estudios previos que sugieren que la variabilidad en estas características puede influir en la presentación clínica y el curso de la enfermedad.43 La recolección de datos demográficos, junto con las manifestaciones clínicas y los resultados de las pruebas de imagen, permitió a los investigadores realizar un análisis integral de la enfermedad.
Por último, se desarrolló un plan de análisis de datos que contempló tanto métodos estadísticos descriptivos como inferenciales. Se utilizaron herramientas como Microsoft Excel y software estadístico para facilitar el procesamiento y la visualización de la información, lo que a su vez ayudó en la interpretación de los resultados y en la extracción de conclusiones. Esto permitió que los investigadores abordaran de manera efectiva las preguntas de investigación planteadas al inicio del estudio.
En resumen, el diseño del proceso fue clave para estructurar la intervención, seleccionar los instrumentos adecuados de recolección de datos y garantizar que la interpretación de los resultados estuviera alineada con los objetivos del estudio. Esto permitió extraer conclusiones precisas sobre el uso de técnicas de imagen en el diagnóstico y seguimiento de la sarcoidosis, contribuyendo al avance del conocimiento en este campo.
Desarrollo del trabajo
En este apartado del estudio se expuso la implementación de acciones y el levantamiento de datos según la metodología seleccionada, ya fuera cualitativa, cuantitativa o de análisis conceptual. Este proceso se reveló esencial para documentar la aplicación de los instrumentos definidos en forma previa, lo que aseguró la recolección de datos relevantes para la investigación.
En un estudio sobre técnicas de imagen en sarcoidosis pulmonar se adoptó una metodología cuantitativa enfocada en la recopilación de datos a partir de imágenes diagnósticas, como radiografías de tórax y tomografías computarizadas de alta resolución (TCAR). A lo largo del desarrollo del trabajo se obtuvieron imágenes en diferentes etapas de la enfermedad, facilitando un análisis comparativo entre los distintos estadios de sarcoidosis.
Las radiografías de tórax fueron útiles para la clasificación inicial de los pacientes, mientras que la TCAR demostró ser más efectiva para detectar cambios parenquimatosos sutiles y complicaciones fibróticas en fases avanzadas.44 Esto se alinea con los objetivos de la investigación, que buscaban identificar métodos diagnósticos precisos para mejorar la evaluación clínica de la sarcoidosis.
La implementación de criterios estandarizados para la interpretación de las imágenes, como el sistema de puntuación de Scadding, también fue fundamental. La recolección de datos en intervalos predefinidos aseguró la consistencia y permitió una evaluación longitudinal del progreso de la enfermedad, facilitando la identificación de patrones evolutivos significativos.45 Esta meticulosidad fue crucial para responder a los objetivos de la investigación, que incluían el seguimiento de la evolución de la sarcoidosis a través de técnicas de imagen.
El desarrollo del trabajo también promovió una interacción multidisciplinaria, donde radiólogos, neumonólogos y otros especialistas revisaron las imágenes y correlacionaron los hallazgos con los síntomas clínicos de los pacientes. Este enfoque colaborativo se llevó a cabo en el Hospital de Agudos Dr. Enrique Tornú, donde se realizaron todos los exámenes de imagen. La colaboración entre distintas especialidades fue clave para asegurar la precisión en el diagnóstico y el seguimiento del estado de salud de los pacientes, lo cual está en línea con los objetivos de la investigación sobre la mejora del manejo clínico de la sarcoidosis.
Finalmente, se realizaron análisis estadísticos para evaluar la eficacia de las diferentes técnicas de imagen en cada fase de la enfermedad. La combinación de análisis descriptivos y comparativos permitió establecer correlaciones significativas entre los hallazgos radiológicos y la progresión clínica de los pacientes, contribuyendo así a una mejor comprensión de la sarcoidosis y su tratamiento.46 Esto refuerza el objetivo principal de la investigación, que era determinar la relación entre las técnicas de imagen y la evolución clínica de la sarcoidosis, con el fin de optimizar el diagnóstico y el manejo de esta enfermedad.
Análisis de resultados
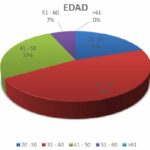
En el período analizado en el Hospital Tornú el 46% (7) de los pacientes con diagnóstico de sarcoidosis tiene una edad entre 30 y 40 años, el 27% (4) tiene entre 40 y 50 años, el 20% (3) tiene entre 20 y 30 años y el 7% (1) entre 50 y 60 años. En cuanto a la distribución de casos de sarcoidosis en relación con la edad se puede interpretar que hay una mayor incidencia de sarcoidosis en el grupo etario de 30 a 40 años, y sugiere que la incidencia de sarcoidosis disminuye a medida que avanza la edad, siendo nula para los pacientes mayores de 60 años.
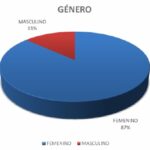
En cuanto a la distribución de género de los pacientes con sarcoidosis en el Hospital Tornú durante los últimos diez años, la proporción de mujeres es de 13/15, lo que representa el 86,7%, y la proporción de hombres fue de 2/15, que representa el 13,3%, es decir que hay aproximadamente 1 hombre por cada 6-7 mujeres con sarcoidosis.
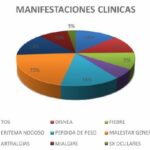
La manifestación clínica más común en los pacientes con sarcoidosis pulmonar fue el “malestar general”, con un total de 15 casos, seguido de la “tos” y la “pérdida de peso”, con diez casos cada una. Por otro lado, las manifestaciones clínicas menos frecuentes fueron el “Sx oculares”, con dos casos, y el “eritema nodoso”, con cuatro casos.
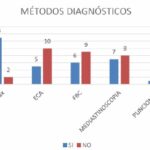
Con relación a los métodos diagnósticos utilizados, se observó que el 100% de los pacientes incluidos en el estudio se sometió a una RX de tórax como parte del proceso de diagnóstico de la sarcoidosis. Además, se encontró que el 86,7% (13 de 15 pacientes) se realizó una TC de tórax. Asimismo, el 33,3% (5 de 15 pacientes) se sometió a un dosaje de ECA como parte del diagnóstico. En cuanto a otros métodos diagnósticos, se encontró que el 46,7% (7 de 15 pacientes) se diagnosticó mediante el uso de la biopsia de piel, mientras que el 40% (6 de 15 pacientes) se realizó mediastinoscopia. Por último, se observó que el 6,7% (1 de 15 pacientes) se sometió a punción con aguja de ganglios para obtener muestras diagnósticas. Estos resultados indican la variabilidad en los métodos diagnósticos utilizados en la identificación de la sarcoidosis en la población estudiada. Todos los pacientes incluidos en el estudio fueron diagnosticados mediante biopsia como parte del proceso de identificación de la sarcoidosis. Esta información resalta la importancia y la fiabilidad de la biopsia en el diagnóstico de la sarcoidosis en la población estudiada.
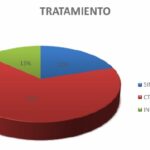
Del total de 15 pacientes analizados, el 80% (12 pacientes) recibió algún tipo de tratamiento para la sarcoidosis. El 20% restante (3 pacientes) no recibió ningún tratamiento. Entre aquellos que recibieron tratamiento, el 83,3% (10 pacientes) fue tratado con corticoides, mientras que el 16,7% (2 pacientes) recibió inmunosupresores. Estos resultados indican que la mayoría de los pacientes con sarcoidosis en el estudio fueron tratados con corticoides, seguido de un menor porcentaje que recibió inmunosupresores como parte de su manejo terapéutico.
La sarcoidosis se caracterizó por ser una enfermedad de causa desconocida, que se desarrolló en personas genéticamente susceptibles, a menudo tras la exposición a agentes ambientales o no ambientales. Esta condición desencadenó una respuesta inmunitaria que resultó en la formación de granulomas no necrotizantes, una de las características distintivas de la enfermedad. La prevalencia de la sarcoidosis varió entre 5 y 40 casos por cada 100.000 habitantes al año, siendo más común en países escandinavos y en la población afronorteamericana. En Latinoamérica la incidencia fue baja, posiblemente debido a la presencia de otras enfermedades granulomatosas endémicas que complicaron el diagnóstico. La literatura científica incluyó diversos estudios que analizaron las características epidemiológicas, diagnósticas y terapéuticas de esta enfermedad.
En este contexto, se compararon los resultados de tres hospitales: el Hospital Favaloro, que revisó retrospectivamente 26 pacientes durante 15 años; el Hospital Británico, que analizó retrospectivamente 24 pacientes con sarcoidosis durante diez años; y el estudio actualmente en curso en el Hospital Tornú.
En términos de distribución por género, el Hospital Tornú encontró una clara predominancia de la sarcoidosis pulmonar en mujeres, con un 86,7% de los casos, un resultado similar al reportado por el Hospital Favaloro, donde el 53,8% de los pacientes eran mujeres. Este hallazgo concordó con múltiples estudios previos que indicaron una mayor incidencia de sarcoidosis en mujeres en diversas poblaciones. Sin embargo, el Hospital Británico no encontró diferencias significativas en la proporción de ambos sexos, lo que sugiere una posible variabilidad en la distribución de género de la enfermedad dependiendo del centro de atención. Es importante destacar que la causa exacta de esta disparidad de género aún no se había establecido con claridad, lo que requería investigaciones adicionales.
En cuanto a la edad de los pacientes, tanto el Hospital Británico como el Hospital Tornú encontraron que el grupo más afectado era el de 31 a 40 años. El Hospital Favaloro reportó una edad media al diagnóstico de 42,6 ± 12,7 años, con un número significativo de pacientes en el grupo de 20 a 30 años. Además, el Hospital Británico no registró casos en pacientes mayores de 60 años, lo que podría indicar una menor incidencia de la enfermedad en este grupo etario. Estos hallazgos coincidieron con la literatura existente, que señala que la sarcoidosis tiene una mayor incidencia en adultos jóvenes, en especial durante la tercera y cuarta década de vida.
Respecto de las manifestaciones clínicas, los síntomas más comunes fueron similares en los tres hospitales, destacando la tos y la disnea como los principales síntomas de presentación. El Hospital Británico también reportó astenia y dolor abdominal como síntomas adicionales, mientras que el Hospital Tornú observó fiebre, eritema nodoso, artralgias, mialgias y síntomas oculares como manifestaciones menos frecuentes. El Hospital Favaloro incluyó pérdida de peso y fiebre entre sus hallazgos clínicos. Es importante señalar que la presencia y gravedad de las manifestaciones clínicas pueden variar considerablemente entre pacientes, lo que resalta la necesidad de una evaluación individualizada y exhaustiva.
En cuanto a los métodos diagnósticos, los tres hospitales utilizaron la radiografía de tórax y la tomografía computarizada (TC) como herramientas diagnósticas principales. Estos hallazgos son consistentes con las guías clínicas actuales, que recomiendan realizar imágenes de tórax como parte del enfoque diagnóstico inicial de la sarcoidosis pulmonar. Adicionalmente, otros métodos, como el dosaje de enzima convertidora de angiotensina (ECA), punción de ganglio extrapulmonar, mediastinoscopia y biopsia de piel, también se utilizaron, aunque en menor proporción. Estos métodos complementarios pueden ser necesarios para confirmar el diagnóstico y evaluar la extensión y gravedad de la enfermedad.
En cuanto al tratamiento, los corticoides fueron la opción más comúnmente utilizada en todos los hospitales, con porcentajes similares en el Hospital Favaloro (69,2% de los casos) y en el Hospital Tornú (66,7% de los casos). El uso de inmunosupresores se reportó en el 11,5% de los casos en el Hospital Favaloro y en el 13,3% en el Hospital Tornú. Además, el Hospital Favaloro mencionó que el 17,4% de los pacientes con afectación pulmonar requirieron oxigenoterapia domiciliaria, y se realizó un caso de trasplante unipulmonar. Estos resultados se alinearon con las recomendaciones actuales, que apoyan el uso de corticosteroides como terapia de primera línea en la sarcoidosis pulmonar sintomática y en casos de afectación pulmonar significativa. La utilización de inmunosupresores en un pequeño porcentaje de pacientes puede indicar la necesidad de una terapia más agresiva en casos graves o refractarios.
Estos hallazgos ofrecieron una visión más completa de la sarcoidosis pulmonar y contribuyeron a una mejor comprensión de esta enfermedad. Se requirieron investigaciones adicionales con muestras más amplias y estudios prospectivos para fortalecer y ampliar estos resultados, así como para profundizar en la comprensión de la sarcoidosis pulmonar y mejorar su diagnóstico y manejo clínico.
Conclusiones y recomendaciones
Conclusiones
A partir del análisis retrospectivo de la población de pacientes con sarcoidosis pulmonar en el Hospital Tornú durante los últimos diez años, se formularon las siguientes conclusiones.
La sarcoidosis pulmonar mostró una mayor prevalencia en mujeres, aunque se observó que la distribución de género podía variar entre diferentes centros de atención.
La causa exacta de esta disparidad no se había establecido claramente, lo que indicaba la necesidad de realizar investigaciones adicionales.
La enfermedad tendió a afectar principalmente a adultos jóvenes, con un pico de incidencia en el grupo de edad entre 31 y 40 años. La incidencia disminuyó de manera notable en pacientes de mayor edad, siendo poco frecuente en personas mayores de 60 años.
La gravedad y la manifestación de síntomas variaron significativamente entre los pacientes, con una mayor prevalencia de síntomas relacionados con la afectación pulmonar en comparación con otros órganos.
Se destacó la importancia de adoptar un enfoque individualizado en el diagnóstico y tratamiento de la sarcoidosis pulmonar, considerando las particularidades de cada paciente.
El diagnóstico de la sarcoidosis pulmonar se fundamentó principalmente en una evaluación clínica exhaustiva, que incluye la revisión de la historia médica del paciente y la realización de un examen físico detallado. No obstante, los métodos de imagen han demostrado ser herramientas cruciales en este proceso diagnóstico. En particular, la tomografía computarizada (TC) ha emergido como una técnica altamente efectiva para la visualización de alteraciones pulmonares asociadas con la sarcoidosis.
La TC permite una evaluación más precisa de las características morfológicas de las lesiones pulmonares, facilitando la identificación de patrones específicos que pueden ser indicativos de la enfermedad. Además, su capacidad para proporcionar imágenes en cortes transversales detallados del tórax permite una mejor apreciación de la extensión y la distribución de los granulomas, así como de las posibles complicaciones asociadas.
Por lo tanto, aunque la evaluación clínica continúa siendo un pilar fundamental en el diagnóstico de la sarcoidosis pulmonar, la integración de técnicas de imagen, en especial la tomografía computarizada, enriquece significativamente el proceso diagnóstico. Esto no solo mejora la precisión del diagnóstico, sino que también puede guiar decisiones terapéuticas y permitir un seguimiento más efectivo de la enfermedad.
Se subrayó la necesidad de llevar a cabo futuras investigaciones con muestras más amplias y estudios prospectivos para fortalecer y ampliar estos hallazgos, contribuyendo así a un mejor conocimiento y manejo clínico de esta compleja enfermedad.
Recomendaciones
Basándonos en los resultados y hallazgos de este estudio sobre la sarcoidosis pulmonar en el Hospital Tornú, se sugirieron las siguientes recomendaciones.
Se propuso continuar con investigaciones prospectivas y estudios que involucraran muestras más grandes para ampliar la comprensión de la sarcoidosis pulmonar y obtener resultados más representativos.
Se recomendó realizar estudios multicéntricos que incluyan diferentes centros médicos y poblaciones, lo que permitiría obtener una visión más amplia y generalizada de la sarcoidosis pulmonar.
Se enfatizó en la importancia de promover la concientización sobre la sarcoidosis pulmonar entre los profesionales de la salud, con el objetivo de mejorar la detección temprana y el diagnóstico preciso de la enfermedad.
Se sugirió establecer protocolos estandarizados para el diagnóstico y seguimiento de los pacientes con sarcoidosis pulmonar, considerando los métodos diagnósticos más efectivos y las opciones de tratamiento disponibles.
Se alentó a fomentar la colaboración multidisciplinaria entre neumólogos, patólogos, radiólogos y otros especialistas, con el fin de abordar de manera integral el diagnóstico y manejo de la sarcoidosis pulmonar.
Notas
1 Baughman, R. P., Teirstein, A. S., Boffa, M. C. et al. (2001). Sarcoidosis. N Engl J Med, 345(26), 1979-1987.
2 Grunewald, J. et al. (2015). Sarcoidosis: a new perspective on an old disease. Nat Rev Dis Primers, 1, 15001.
3 Moller, D. R. et al. (2009). Sarcoidosis: an overview. Clin Chest Med, 30(4), 597-614.
4 Wang, X. et al. (2017). The role of imaging in the management of sarcoidosis. Clin Respir J, 11(4), 471-481.
5 Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
6 Idem.
7 Idem.
8 Valeyre, D., Prasse, A., & Nunes, H. (2014). Sarcoidosis. The Lancet, 383(9923), 1155-1167.
9 Idem.
10 Nunes, H., Sanyal, S., & Valeyre, D. (2015). Serum angiotensin converting enzyme as a marker of disease activity in sarcoidosis: a review. European Respiratory Journal, 46(5), 1352-1361.
11 Hunninghake, G. W. et al. (2017). The role of angiotensin converting enzyme in sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 38(4), 405-411.
12 Idem.
13 Grunewald, J., Eklund, A., & Olin, A. C. (2014). Serum angiotensin-converting enzyme and the clinical course of sarcoidosis. Chest, 146(3), 533-540.
14 Iannuzzi, M. C., & Rybicki, B. A. (2007). The epidemiology of sarcoidosis. Chest, 131(2), 459-467.
15 Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
16 Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
17 Casas, M. et al. (2021). Intercambio de Presentaciones sobre Radiología.
18 Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
19 Sharma, O. P., Johnson, R. H. (1982). The radiographic staging of sarcoidosis: a reappraisal. Am J Roentgenol, 139(5), 895-899.
20 Ohara, T., Inoue, Y., Nakajima, T., Ohsawa, H., Komada, T., Harada, H. et al. (2016). Pulmonary sarcoidosis: comparison of findings of inspiratory and expiratory high-resolution CT and pulmonary function tests between smokers and nonsmokers. J Thorac Imaging, 31(2), 119-126.
21 Nunes, H., Humbert, M., Capron, F., Brauner, M. W., Sitbon, O., Battesti, J. P. et al. (2007). CT and FDG PET in the assessment of response to treatment in severe pulmonary sarcoidosis. Thorax, 62(1), 62-67.
22 Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
23 Casas, M. et al. (2021). Intercambio de Presentaciones sobre Radiología.
24 Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
25 Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
26 Scadding, J. G. (1961). Prognosis of intrathoracic sarcoidosis in England. BMJ, 2(5261), 1165-1172.
27 Criado, E., Sánchez, M., Ramírez, J., Arguis, P., De Caralt, T. M., Perea, R. J. et al. (2010). Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation. Radiographics, 30(6), 1567-1586.
28 Keijsers, R. G., Grutters, J. C., Thomeer, M., Van Den Bosch, J. M., Gietema, H. A. (2013). Imaging the inflammatory activity of sarcoidosis. Eur Respir J, 41(3), 743-751.
29 Arkema, E. V., Cozier, Y. C. (2018). Epidemiology of sarcoidosis: current findings and future directions. Ther Adv Chronic Dis, 9(11), 227-240.
30 Universidad Nacional Autónoma de México (2023). Uso de Técnicas de Imagen en el Diagnóstico y Seguimiento de la Sarcoidosis Pulmonar. Tesis de Postgrado en Neumología.
31 Hospital General de México (2023). Eficacia de Técnicas de Imagen en la Identificación de Sarcoidosis Pulmonar.
32 Universidad de Barcelona (2023). El Papel de la PET en el Seguimiento de Pacientes con Sarcoidosis Pulmonar.
33 Hess, D. R. (2004). Retrospective studies and chart reviews. Respir Care, 49(10), 1171.
34 Simon, R., Freidlin, B., Rubinstein, L., Arbuck, S. G., Collins, J., Christian, M. C. (1997). Accelerated titration designs for phase I clinical trials in oncology. J Natl Cancer Inst, 1989(15), 1138-1147.
35 Judson, M. A. (2008). The diagnosis of sarcoidosis. Clin Chest Med, 29(3), 415-427.
36 Marten, K., Milne, D., Hansell, D. M. (2003). Pulmonary sarcoidosis: radiological findings. Clin Radiol, 58(8), 533-543.
37 Scadding, J. G. (1961). Prognosis of intrathoracic sarcoidosis in England. BMJ, 2(5261), 1165-1172.
38 Criado, E., Sánchez, M., Ramírez, J., Arguis, P., De Caralt, T. M., Perea, R. J. et al. (2010). Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation. Radiographics, 30(6), 1567-1586.
39 Baughman, R. P., Lower, E. E., du Bois, R. M. (2003). Sarcoidosis. Lancet, 361(9363), 1111-1118.
40 Pérez-Alonso, M., García-López, F., Sánchez-López, J. (2018). Diagnóstico de enfermedades respiratorias a través de imágenes. Rev Med Respir, 34(2), 135-142.
41 Rodríguez, L., Fernández, R., López, E. (2020). Técnicas de imagen en sarcoidosis: comparación entre radiografía y TCAR. Radiol Pulm, 45(3), 290-295.
42 Gómez-Sánchez, M. (2017). Estrategias diagnósticas en la evaluación de pacientes con enfermedades intersticiales pulmonares. Interés J Diagnóstico, 12(4), 207-212.
43 Martínez-Cannon, B., Torres, M., Ramos. P. (2019). Factores demográficos y clínicos en la sarcoidosis: un análisis de cohortes. Arch Bronconeumol, 55(1), 34-40.
44 Rodríguez-Martínez, P., García-Moreno. J, Sánchez-López, M. (2019). Evaluación de las técnicas de imagen en la sarcoidosis pulmonar: un enfoque longitudinal. Rev Radiol Torac, 28(3), 156-163.
45 González-Pérez, F. (2020). Técnicas de imagen en la evaluación de enfermedades intersticiales: radiografía y tomografía comparada. J Clin Pulmonol,15(4), 215-223.
46 Martínez-López, G. (2018). Eficacia de las técnicas de imagen en el diagnóstico de sarcoidosis pulmonar. Diagnóstico Radiol, 34(2), 102-110.
Referencias bibliográficas
- Baughman, R. P., Teirstein, A. S., Boffa, M. C. et al. (2001). Sarcoidosis. N Engl J Med, 345(26), 1979-1987.
- Grunewald, J. et al. (2015). Sarcoidosis: a new perspective on an old disease. Nat Rev Dis Primers, 1, 15001.
- Moller, D. R. et al. (2009). Sarcoidosis: an overview. Clin Chest Med, 30(4), 597-614.
- Wang, X. et al. (2017). The role of imaging in the management of sarcoidosis. Clin Respir J, 11(4), 471-481.
5, 6, 7, 8. Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
- Valeyre, D., Prasse, A., & Nunes, H. (2014). Sarcoidosis. The Lancet, 383(9923), 1155-1167.
- Valeyre, D., Prasse, A., & Nunes, H. (2014). Sarcoidosis. The Lancet, 383(9923), 1155-1167.
- Nunes, H., Sanyal, S., & Valeyre, D. (2015). Serum angiotensin converting enzyme as a marker of disease activity in sarcoidosis: a review. European Respiratory Journal, 46(5), 1352-1361.
- Hunninghake, G. W. et al. (2017). The role of angiotensin converting enzyme in sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 38(4), 405-411.
- Hunninghake, G. W. et al. (2017). The role of angiotensin converting enzyme in sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 38(4), 405-411.
- Grunewald, J., Eklund, A., & Olin, A. C. (2014). Serum angiotensin-converting enzyme and the clinical course of sarcoidosis. Chest, 146(3), 533-540.
- Iannuzzi, M. C., & Rybicki, B. A. (2007). The epidemiology of sarcoidosis. Chest, 131(2), 459-467.
- Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
- Casas, M. et al. (2021). Intercambio de Presentaciones sobre Radiología.
- Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
- Sharma, O. P., Johnson, R. H. (1982). The radiographic staging of sarcoidosis: a reappraisal. Am J Roentgenol, 139(5), 895-899.
- Ohara, T., Inoue, Y., Nakajima, T., Ohsawa, H., Komada, T., Harada, H. et al. (2016). Pulmonary sarcoidosis: comparison of findings of inspiratory and expiratory high-resolution CT and pulmonary function tests between smokers and nonsmokers. J Thorac Imaging, 31(2), 119-126.
- Nunes, H., Humbert, M., Capron, F., Brauner, M. W., Sitbon, O., Battesti, J. P. et al. (2007). CT and FDG PET in the assessment of response to treatment in severe pulmonary sarcoidosis. Thorax, 62(1), 62-67.
- Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
- Casas, M. et al. (2021). Intercambio de Presentaciones sobre Radiología.
- Fauci, A. S., Harrison, T. R. (2012). Principles of Internal Medicine.
- Naranjo, C. et al. (2022). Revista Sanitaria de Investigación.
- Scadding, J. G. (1961). Prognosis of intrathoracic sarcoidosis in England. BMJ, 2(5261), 1165-1172.
- Criado, E., Sánchez, M., Ramírez, J., Arguis, P., De Caralt, T. M., Perea, R. J. et al. (2010). Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation. Radiographics, 30(6), 1567-1586.
- Keijsers, R. G., Grutters, J. C., Thomeer, M., Van Den Bosch, J. M., Gietema, H. A. (2013). Imaging the inflammatory activity of sarcoidosis. Eur Respir J, 41(3), 743-751.
- Arkema, E. V., Cozier, Y. C. (2018). Epidemiology of sarcoidosis: current findings and future directions. Ther Adv Chronic Dis, 9(11), 227-240.
- Universidad Nacional Autónoma de México (2023). Uso de Técnicas de Imagen en el Diagnóstico y Seguimiento de la Sarcoidosis Pulmonar. Tesis de Postgrado en Neumología.
- Hospital General de México (2023). Eficacia de Técnicas de Imagen en la Identificación de Sarcoidosis Pulmonar.
- Universidad de Barcelona (2023). El Papel de la PET en el Seguimiento de Pacientes con Sarcoidosis Pulmonar.
- Hess, D. R. (2004). Retrospective studies and chart reviews. Respir Care, 49(10), 1171. Judson, M. A. (2008). The diagnosis of sarcoidosis. Clin Chest Med, 29(3), 415-427.
- Simon, R., Freidlin, B., Rubinstein, L., Arbuck, S. G., Collins, J., Christian, M. C. (1997). Accelerated titration designs for phase I clinical trials in oncology. J Natl Cancer Inst, 1989(15), 1138-1147.
- Judson, M. A. (2008). The diagnosis of sarcoidosis. Clin Chest Med, 29(3), 415-427.
- Marten, K., Milne, D., Hansell, D. M. (2003). Pulmonary sarcoidosis: radiological findings. Clin Radiol, 58(8), 533-543.
- Scadding, J. G. (1961). Prognosis of intrathoracic sarcoidosis in England. BMJ, 2(5261), 1165-1172.
- Criado, E., Sánchez, M., Ramírez, J., Arguis, P., De Caralt, T. M., Perea, R. J. et al. (2010). Pulmonary sarcoidosis: typical and atypical manifestations at high-resolution CT with pathologic correlation. Radiographics, 30(6), 1567-1586.
- Baughman, R. P., Lower, E. E., du Bois, R. M. (2003). Sarcoidosis. Lancet, 361(9363), 1111-1118.
- Pérez-Alonso, M., García-López, F., Sánchez-López, J. (2018). Diagnóstico de enfermedades respiratorias a través de imágenes. Rev Med Respir, 34(2), 135-142.
- Rodríguez, L., Fernández, R., López, E. (2020). Técnicas de imagen en sarcoidosis: comparación entre radiografía y TCAR. Radiol Pulm, 45(3), 290-295.
- Gómez-Sánchez, M. (2017). Estrategias diagnósticas en la evaluación de pacientes con enfermedades intersticiales pulmonares. Interés J Diagnóstico, 12(4), 207-212.
- Martínez-Cannon, B., Torres, M., Ramos. P. (2019). Factores demográficos y clínicos en la sarcoidosis: un análisis de cohortes. Arch Bronconeumol, 55(1), 34-40.
- Rodríguez-Martínez, P., García-Moreno. J, Sánchez-López, M. (2019). Evaluación de las técnicas de imagen en la sarcoidosis pulmonar: un enfoque longitudinal. Rev Radiol Torac, 28(3), 156-163.
- González-Pérez, F. (2020). Técnicas de imagen en la evaluación de enfermedades intersticiales: radiografía y tomografía comparada. J Clin Pulmonol,15(4), 215-223.
- Martínez-López, G. (2018). Eficacia de las técnicas de imagen en el diagnóstico de sarcoidosis pulmonar. Diagnóstico Radiol, 34(2), 102-110.
Glosario
Biopsia: procedimiento diagnóstico en el que se extrae una muestra de tejido para su análisis histopatológico.
Corticoides: medicamentos antiinflamatorios que imitan los efectos de las hormonas producidas por las glándulas suprarrenales, utilizados comúnmente en el tratamiento de enfermedades autoinmunes y de inflamación.
Disnea: dificultad para respirar o sensación de falta de aire.
ECA (enzima convertidora de angiotensina): enzima que se mide en sangre y que puede estar elevada en pacientes con sarcoidosis, utilizada como uno de los métodos diagnósticos.
Epidemiología: estudio de la distribución y determinantes de la salud y enfermedades en poblaciones específicas.
Granulomas: agrupaciones de células inmunitarias que se forman en respuesta a la inflamación crónica, característicos de la sarcoidosis.
Inmunosupresores: medicamentos que reducen la respuesta del sistema inmunitario, utilizados en el tratamiento de enfermedades autoinmunes y en casos severos de sarcoidosis.
Mediastinoscopia: procedimiento quirúrgico para examinar el mediastino (la región entre los pulmones) y obtener muestras de tejido.
Radiografía de tórax: técnica de imagen que utiliza rayos X para visualizar el interior del tórax, fundamental en el diagnóstico de enfermedades pulmonares.
Sarcoidosis: enfermedad inflamatoria de causa desconocida, caracterizada por la formación de granulomas en distintos órganos, especialmente en los pulmones.
Síntomas clínicos: manifestaciones de una enfermedad que se pueden observar o describir, como tos, fiebre y pérdida de peso.
TCAR (tomografía computarizada de alta resolución): técnica de imagen que proporciona cortes detallados del tórax, utilizada para evaluar la afectación pulmonar en sarcoidosis.
Trasplante pulmonar: procedimiento quirúrgico que implica reemplazar uno o ambos pulmones por pulmones sanos de un donante, utilizado en casos avanzados de enfermedades pulmonares.