Autora
Dr. Oscar David Negrete Romero (Sanatorio Franchín, Capital Federal, Argentina).
Tutor
Dr. Gustavo San Martin (Sanatorio Franchín, Capital Federal, Argentina)
Epígrafes
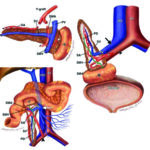
Fig. 1: Drenaje venoso portal (flecha blanca). Drenaje venoso sistémico a la vena iliaca (flecha negra). Anastomosis a la arteria iliaca (punta de flecha). Duodeno (excreción a yeyuno / excreción a vejiga) (*).
Fig. 2: Anastomosis de la vena mesentérica sup. del donante con la vena mesentérica sup. a vena porta del receptor.
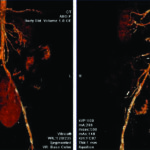
Fig. 3. Angio TC. Reconstrucción en 3D.
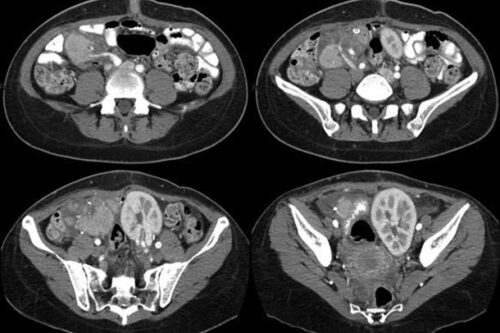
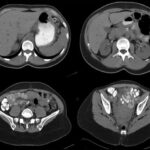
Fig. 4. TC preoperatoria, cortes coronales y sagitales. No se observan alteraciones significativas en el sistema vascular.
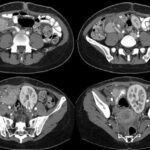
Fig. 5. TC post operatoria: cortes coronales y sagitales.
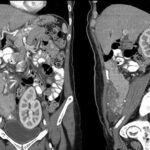
Fig. 6. TC preoperatoria.
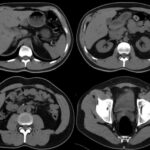
Fig. 7. TC post operatoria.
Fig. 8. TC post operatoria, un mes posterior a la cirugía.
OBJETIVO GENERAL
Ampliar el conocimiento del especialista en diagnóstico por imágenes sobre el trasplante pancreático, destacar su aporte como parte de un equipo multidisciplinario y la importancia de estar al tanto de la evolución en las distintas técnicas quirúrgicas para realizar un adecuado seguimiento pre y post operatorio en imágenes y adquirir las bases teóricas necesarias que ayuden en la evaluación práctica de estos pacientes.
OBJETIVO ESPECÍFICOS
- Revisión y actualización bibliográfica sobre el trasplante pancreático;
- Descripción de los hallazgos por tomografía computada multidetector (TCMD) que indican complicación en el trasplante pancreático;
- Clasificar las complicaciones que se presentan en estos pacientes.
INTRODUCCIÓN
El objetivo de este trabajo es ampliar el conocimiento como médicos radiólogos acerca de los nuevos procedimientos en trasplante pancreático y sobre el avance de las distintas especialidades médicas en el tema. La gran evolución del trasplante renopancreático de los últimos años obliga al imagenólogo a conocer las distintas complicaciones que puede plantear esta cirugía y a contar con las herramientas que le permitan su detección a tiempo a fin de posibilitar una adecuada y oportuna comunicación con el médico tratante en beneficio del paciente trasplantado.
Este tipo de cirugías permite en muchos casos mejorar las perspectivas en enfermedades tan prevalentes como la diabetes y la insuficiencia renal, con todas sus complicaciones asociadas, posibilitando que el paciente suspenda aplicaciones exógenas de insulina o, en otros casos, que disminuya la frecuencia de hemodiálisis. Tanto la eficacia de los nuevos tratamientos inmunosupresores como el adecuado reconocimiento de los pacientes susceptibles de ser sometidos a esta cirugía y las distintas variantes en la técnica quirúrgica son factores determinantes en estos casos. El papel de las imágenes, principalmente de la TCMD, es fundamental para la rápida detección de posibles complicaciones y evitar el fracaso quirúrgico, ocupando también el eco Doppler un lugar muy importante, en muchos casos definitorio, en el seguimiento posquirúrgico.
MARCO TEÓRICO
Las mejoras en las técnicas quirúrgicas y los tratamientos inmunodepresores han aumentado la tasa de éxito del trasplante de páncreas mediante aloinjerto en humanos, que se realiza generalmente en casos seleccionados de diabetes mellitus tipo 1. Prácticamente el 90% de estos casos implican un trasplante simultáneo de páncreas y riñón del mismo donante; otras técnicas utilizadas, pero menos frecuentes, son el trasplante de páncreas tras el trasplante de riñón y el trasplante aislado de páncreas.
El conocimiento del método quirúrgico y la anatomía radiológica posquirúrgica es fundamental para el seguimiento y el diagnóstico de las complicaciones. Es indispensable conocer la reconstrucción arterial que implica la anastomosis de la arteria esplénica y la arteria mesentérica superior del donante con la arteria ilíaca común o externa del receptor mediante un injerto de extensión en “Y” de la arteria ilíaca del donante. El drenaje venoso sistémico implica la anastomosis de la vena portal del donante con la vena ilíaca del receptor (Fig. 1) (1).
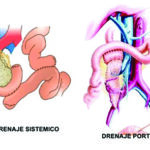
El drenaje venoso portal se realiza mediante anastomosis de la vena mesentérica superior del donante con la vena mesentérica superior o la vena porta del receptor (Fig. 2) (2).
El antiguo método de drenaje de las secreciones exocrinas a través de la vejiga está siendo sustituido por un drenaje entérico, más fisiológico, hacia el yeyuno.
Las principales complicaciones en estos procedimientos incluyen problemas técnicos como la trombosis vascular y las fugas en las anastomosis, el rechazo agudo y crónico, la pancreatitis, la formación de pseudoquistes, hematomas, abscesos y la infección. El rechazo del aloinjerto es difícil de controlar debido a los signos y síntomas inespecíficos, la relativa insensibilidad del aumento de los niveles de glucosa y el riesgo de la biopsia pancreática.
Los síntomas leves inespecíficos pueden ser los más precoces o los únicos del rechazo, lo cual indica la necesidad del tratamiento antirrechazo que consiste en aumentar el tratamiento con el inmunosupresor. Pero un tratamiento inmunosupresor excesivo en un paciente que no presenta rechazo es un riesgo innecesario de morbilidad y mortalidad debido a infecciones, neurotoxicidad y supresión de la médula ósea. Además, es complejo seguir la evolución del rechazo, porque su resolución no produce un cambio significativo en los síntomas o los resultados de laboratorio.
En la tomografía computada (TC), la glándula trasplantada se muestra heterogénea y tiene un mayor tamaño, con líquido y hemorragia circundantes en la fase postrasplante precoz (<4 semanas). Por tanto, es necesario un estudio basal pretratamiento para diferenciar los cambios del rechazo o la pancreatitis de los cambios postrasplante. Los grados variables de heterogeneidad de heterogeneidad en el tejido trasplantado y la inflamación peripancreática en la TC, acompañados de un nivel elevado de amilasa y de sensibilidad dolorosa en el aloinjerto, son hallazgos inespecíficos; pueden observarse en los pacientes con rechazo precoz al trasplante o en aquellos con pancreatitis.
La TC es útil para la detección de acumulaciones intraabdominales de líquido asociadas al trasplante, pero la diferenciación de las acumulaciones estériles de las infecciosas requiere una aspiración percutánea.
El contraste EV es importante para la detección y la evaluación de las complicaciones vasculares (angioTC) y para la documentación de la necrosis pancreática, que es la fase terminal de la lesión isquémica de la glándula. Se pueden hacer reconstrucciones en 3D que son muy útiles para el análisis conjunto con los cirujanos tratantes (Fig. 3) (3).
La atrofia pancreática puede ser un hallazgo tardío en una glándula con una función endocrina normal y un rechazo crónico. La alteración de la función endocrina es un indicador poco sensible y puede no estar presente hasta las últimas fases del rechazo.
La resonancia magnética (RM) ha mostrado ser más prometedor a en la detección del rechazo del aloinjerto, posiblemente debido a su mayor sensibilidad a los cambios en el parénquima pancreático. Aunque los hallazgos de la RM pueden no ser siempre obvios, la comparación con los estudios previos es fundamental para diferenciar entre el rechazo agudo y la fase precoz del rechazo agudo. Tras la fase postrasplante inicial, la glándula se muestra hiperintensa respecto a los órganos adyacentes en las imágenes potenciadas en T1 y supresión grasa y capta contraste de forma ávida y uniforme, de forma similar al páncreas normal. La RM muestra áreas multifocales de alteración de la intensidad de señal en las imágenes potenciadas en T1 y T2, con una menor captación de contraste en el caso de rechazo.
Estos hallazgos son detectables incluso antes de que se evidencien las manifestaciones clínicas. Estas áreas tienden a resolverse en pocas semanas con la recuperación del rechazo agudo. También puede haber formación de seudoquistes y hemorragias. Pueden resolverse en pocas semanas con tratamiento y dar lugar a áreas con baja intensidad de señal en las imágenes potenciadas en T1 y en T2, presumiblemente debido a la fibrosis o al depósito de hemosiderina. El rechazo crónico con atrofia glandular produce una baja intensidad de señal en las imágenes potenciadas en T1 y T2, que es compatible con la apariencia típica en la RM del tejido fibroso. La trombosis venosa o arterial se aprecia como un trombo de baja intensidad de señal rodeado de un vaso que capta contraste o como una ausencia de realce en la angioRM. La ausencia de captación de contraste de la glándula trasplantada en el contexto de una trombosis representa un infarto del injerto.
Una disminución del flujo sanguíneo y unos vasos de pequeño calibre en la angioRM pueden preceder a los cambios en la intensidad de señal debido al rechazo. La pancreatitis de la glándula trasplantada se aprecia de forma similar a la nativa y se manifiesta como un aumento de tamaño del páncreas y una inflamación peripancreática (4).
MATERIALES Y MÉTODOS
Como criterios de inclusión de pacientes en el tratamiento de trasplante se consideran (5):
- Diabetes mellitus tipo 1 preferentemente;
- Edad: < 50 años;
- Péptido C: < 0.5 ng/ml;
- Filtración glomerular: < 40 ml/min;
- Ausencia de cardiopatía coronaria o tratada con revascularización;
- Ausencia de enfermedad vascular obstructiva severa con riesgo de isquemia de las extremidades inferiores;
- Ausencia de neuropatía motora o autonómica incapacitante.
Los criterios para el donante son los siguientes:
- Edad: 15 – 45 años;
- IMC: < 30 kg/m2;
- Peso mínimo: 30 kg;
- Sodio plasmático: < 130 U/l;
- Lipasa: < 160 U/l;
- Sin historia de diabetes mellitus;
- Sin historia de alcoholismo;
- Ausencia de traumatismo abdominal severo;
Se analizaron los estudios de TCMD de dos pacientes sometidos a control post quirúrgico de trasplante renopancreático en el Sanatorio Franchin en el año 2015.
El diagnóstico de diabetes se basó en los antecedentes aportados por el médico tratante y en los valores de laboratorio de las historias clínicas: valores de la glucemia en ayunas (140 mg/dl o más) o en la prueba de tolerancia a la glucosa oral (glucemia en plasma venoso igual o superior a 200 mg/dl a las 2 horas de una sobrecarga oral de glucosa de 75 g). El equipo utilizado fue un tomógrafo Toshiba Aquilion de 64 detectores con capacidad para ampliar a 128. Se administró contraste EV Lobitridol (75ml) (Xenetix 350©) con catéter 18 periférico a una dosis no mayor de 2 ml x kg del paciente, a una velocidad de 4 cc/min con adquisición de imágenes a los 20 segundos para obtener el estudio en tiempo arterial, a los 50 segundos para un tiempo portal y a los 2 minutos para la excreción.
El análisis de las tomografías realizadas fue realizado con un programa de visualización de imágenes VITREA por el jefe de servicio y el grupo de médicos radiólogos de nuestra institución.
Se practicó un estrecho seguimiento de la evolución de los pacientes con el médico cirujano tratante para corroborar la clínica y el desenlace de los mismos. Se consultó y recopiló material bibliográfico relacionado con el tema, rescatando información y trabajos recientes.
En cuanto a la técnica quirúrgica practicada por el cirujano tratante, dato indispensable para una mejor y eficaz valoración de las imágenes, incluyó la anastomosis de la arteria mesentérica superior y la arteria esplénica del donante con la arteria ilíaca externa del receptor mediante un injerto de extensión en Y de la arteria ilíaca del donante. El drenaje venoso sistémico se realizó con la anastomosis de la vena porta del donante con la vena ilíaca del receptor.
Para el drenaje de las secreciones exocrinas, el cirujano tratante optó por el drenaje entérico hacia el yeyuno, más fisiológico, y que presenta menos efectos colaterales, como infecciones urinarias e irritación, que el drenaje hacia la vejiga, que puede provocar esos trastornos.
Caso 1
Paciente de sexo femenino de 38 años de edad, con diagnóstico de diabetes tipo 1, sin antecedente de hemodiálisis previo. Se le realizó tomografía de abdomen y pelvis simple preoperatoria para descartar calcificaciones vasculares, posible causal de complicaciones en las anastomosis de los órganos a trasplantar con las arterias iliacas (Fig. 4). No presentaba alteraciones significativas en el sistema vascular.
Los valores de glucemia (210 mg/ dl), amilasa (460 U/L) y lipasa (270 U/L) aumentados post cirugía, además del dolor abdominal y distensión que presentaba la paciente, motivaron la indicación de una TCMD con contraste EV post operatoria (Fig. 5).
Caso 2
Paciente de sexo masculino de 40 años de edad, diabético tipo 1, sin hemodiálisis. Presentó una tomografía preoperatoria sin calcificaciones en la pared del sistema vascular (Fig. 6). El paciente manifestó dolor abdominal y presentó fiebre posterior al acto quirúrgico, lo cual determinó la realización de una TCMD con contraste EV (Fig. 7). Los niveles de laboratorio post operatorio de glucemia, lipasa y amilasa fueron: 148mg/dl, 37 U/L y 150 U/L, respectivamente.
DISCUSIÓN
En el caso Nº 1, la TC mostró presencia de líquido y alteración de la grasa peripancreática del órgano trasplantado, como así también líquido en los recesos pelvianos, característico de pancreatitis. La evolución clínica y la correlación con el laboratorio clínico confirmaron estos hallazgos. Como tratamiento se indicó reposo digestivo, observándose en los 10 días posteriores a la tomografía considerable mejora clínica y disminución de los valores de laboratorio. Se dio el alta al paciente con una glucemia de 76 mg/dl y una creatinina de 1.1 mg/dl.
En el caso Nº 2, las imágenes mostraron trasplante pancreático en fosa iliaca y flanco derecho, con permeabilidad de las arterias mesentéricas pancreáticas, anastomosadas sin alteraciones a nivel de la arteria iliaca derecha y sin cambios significativos ni defectos de relleno de las estructuras venosas. Tampoco se observaron alteraciones en el asa duodenal interpuesta entre la vejiga y el neopáncreas.
Sin embargo, a pesar de la aparente normalidad del estudio tomográfico realizado, la evolución del paciente fue tórpida, con dolor abdominal muy agudo y cuadros febriles, por lo que fue reintervenido quirúrgicamente, realizándose resección de la cabeza del páncreas por necrosis y fístula. Se diagnosticó pancreatitis por punción y biopsia.
Este caso presentó, además, infección del trasplante renal por virus BK (VBK), perteneciente a la familia de los poliomavirus junto con otros poliomavirus detectados en la especie humana. El VBK se asocia con dos complicaciones en receptores de trasplante: nefropatía asociada a poliomavirus BK (NAPBK) en trasplante renal y cistitis hemorrágica en trasplante de médula ósea. Hay que tener en cuenta esta complicación ya que lleva a la pérdida del órgano trasplantado en más del 50% de los pacientes sometidos a cirugía.
Puntos claves en relación con esta complicación pueden ser:
- La potente y moderna inmunosupresión, que puede ser la responsable de la creciente prevalencia de esta infección;
- La infección por virus BK en pacientes inmunocomprometidos puede afectar a la función y supervivencia del injerto renal;
- El diagnóstico precoz mediante la monitorización estrecha del recuento de células señuelo en orina y viremia es crucial para evitar el impacto negativo de esta complicación;
- No existen evidencias sobre un tratamiento específico efectivo para esta infección. Sólo la reducción de la inmunosupresión minimiza su virulencia(6).
En la segunda tomografía control efectuada se evidenció una disminución en el calibre de la anastomosis arterial, lo que se correlacionó con vasculitis. Con posterioridad a las complicaciones descritas, el paciente presentó los siguientes niveles de laboratorio: glucemia de 88 mg/dl y creatinina de 1.34 mg/dl.
CONCLUSIÓN
Este trabajo refleja la importancia para el radiológico de conocer la evolución de las distintas especialidades médicas y de los nuevos procedimientos quirúrgicos y sus complicaciones y de la necesidad de estar en contacto con los especialistas que interactúan con el servicio de imágenes. En los dos casos presentados, la interpretación de cambios sutiles, como el leve aumento de líquido peripancreático y la alteración de la grasa regional, su correlación con un laboratorio alterado y con la clínica como pilar fundamental, permitieron el arribo al diagnóstico de pancreatitis. No obstante, el segundo caso planteado demostró que la ausencia de una franca alteración en el laboratorio no es excluyente de complicaciones, lo que determina que, según la experiencia del cirujano tratante y lo que refleja la literatura, es fundamental poner énfasis en el seguimiento estricto de la evolución del paciente, proceso en el que el especialista en diagnóstico por imágenes debe ser parte activa, ya que es una pieza clave en la detección temprana de alteraciones patológicas agudas, permitiendo el éxito y evitando en muchas oportunidades el fracaso de procedimientos tan complejos como los presentados en este trabajo.
Bibliografía
- Vandermeer FQ, Manning MA, Frazier AA, Wong-You- Cheong JJ. Imaging of whole-organ pancreas transplants. Radiographics. 2012;32(2):411-35.
- Haaga JR. TC y RM Diagnóstico por imágenes del cuerpo humano. 5ª Ed. Madrid: Elsevier. 2011: pp. 1665.
- Zehnder C. Trasplante de páncreas tipos, selección de receptores y donantes. Rev. Med. Clin. Condes. 2010;21(2):214–217.
- Yuh WT, Hunsicker LG, Nghiem DD, et al. Pancreatic trasplants: Evaluation with MR imaging. Radiology.1989;170(1):171-7.
- Sollinger HW, Stratta RJ, Kalayoglu M, Belzer FO. The University of Wisconsin experience in pancreas transplantation. Transplant Proc.1987;19(4-Suppl 4):48-54.
- Webb R. Fundamentos de TAC body. 3ra Ed. España: Ed. Marbán. 2007.