Resumen
Este artículo ilustra patrones representativos de lesiones mesencefálicas, pontinas y bulbares, mediante una serie de casos con énfasis en la correlación anatómico-imagenológica. Se analizan los patrones de resonancia magnética, particularmente las secuencias de difusión, la topografía de las lesiones y su relación con territorios vasculares específicos. La integración de estos hallazgos permite una caracterización sindrómica precisa y refuerza el valor de la neuroimagen en el diagnóstico diferencial de las lesiones del tronco encefálico.
Palabras clave: tronco encefálico, infarto del tronco encefálico, resonancia magnética, difusión, síndromes del tronco encefálico.
Abstract
This article illustrates representative patterns of midbrain, pontine, and medullary lesions through cases with emphasis on anatomo-radiological correlation. Magnetic resonance imaging patterns are analyzed, particularly diffusion-weighted sequences, lesion topography, and their relationship with specific vascular territories. Integration of these findings allows accurate syndromic characterization and reinforces the role of neuroimaging in the differential diagnosis of brainstem lesions.
Keywords: brainstem, brainstem infarction, magnetic resonance imaging; diffusion-weighted imaging, brainstem syndromes.
Introducción
El tronco encefálico constituye una de las regiones más complejas y funcionalmente críticas del sistema nervioso central. Integrado por mesencéfalo, protuberancia y bulbo raquídeo, alberga numerosos núcleos de nervios craneales, vías ascendentes y descendentes, y centros reguladores esenciales. Debido a esta organización densa, lesiones focales incluso pequeñas pueden generar síndromes neurológicos distintivos cuya identificación precisa representa un desafío diagnóstico, particularmente desde el punto de vista neurorradiológico.
En la práctica clínica, los síndromes del tronco encefálico se asocian con mayor frecuencia a eventos vasculares de la circulación posterior, aunque también pueden originarse por procesos inflamatorios, desmielinizantes, infecciosos o tumorales. La resonancia magnética, en especial mediante secuencias de difusión, permite identificar correlatos anatómicos sutiles y patrones topográficos característicos que facilitan la clasificación sindrómica y la correlación con territorios vasculares específicos.
Aunque los accidentes cerebrovasculares del tronco encefálico representan aproximadamente el 10-12% de todos los ictus isquémicos, su impacto clínico es desproporcionadamente alto debido a la concentración de estructuras vitales en esta región. Las lesiones troncoencefálicas adquieren relevancia particular por su elevada mortalidad y por el riesgo significativo de discapacidad severa.(1) La correcta interpretación imagenológica resulta fundamental para el diagnóstico precoz y la estratificación sindrómica.
El análisis sistemático de la localización y extensión dorsoventral de las lesiones en resonancia magnética ofrece un enfoque pragmático y anatómicamente fundamentado para la diferenciación de los principales síndromes del tronco encefálico. Esta serie de casos presenta una revisión de los principales síndromes del tronco encefálico, con énfasis en la correlación anatómico-imagenológica, ilustrando cómo la evaluación estructurada de los patrones lesionales, en conjunto con su distribución vascular, permite una caracterización sindrómica confiable, incluso en escenarios de presentación clínica incompleta.
Presentación de casos
Caso 1
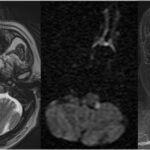
La lesión se localiza en la porción dorsolateral del bulbo raquídeo, generalmente en el territorio irrigado por la arteria cerebelosa posteroinferior, identificable en resonancia magnética como un foco hiperintenso en secuencias T2 y FLAIR, con restricción a la difusión y disminución de la señal en el mapa ADC en la fase aguda. La afectación del pedúnculo cerebeloso inferior y de los núcleos vestibulares, habitualmente en el bulbo lateral rostral, explica el vértigo y la ataxia ipsilateral, mientras que el compromiso del núcleo y tracto espinal del nervio trigémino, de disposición posterolateral, se traduce en pérdida de la sensibilidad termoalgésica facial ipsilateral. En lesiones con mayor extensión medial o caudal, puede observarse compromiso del núcleo ambiguo, con disfagia y disfonía(3) y cuando se afectan las fibras simpáticas descendentes se asocia la aparición de síndrome de Horner ipsilateral. La afectación combinada de estas estructuras explica el patrón sindrómico característico del síndrome de Wallenberg, diferenciándolo de otros infartos medulares con compromiso medial o ventral. Asimismo, se ha descrito que los pacientes con infartos bulbares laterales presentan alteraciones faríngeas más severas que aquellos con infartos hemisféricos, subrayando la importancia de la localización anatómica precisa en la interpretación imagenológica del cuadro clínico.(4) En el momento del inicio, hasta un 50-70% de los pacientes presentan síntomas vestibulares y alteraciones sensitivas cruzadas,(2) hallazgos coherentes con la topografía observada en la resonancia magnética.
Caso 2
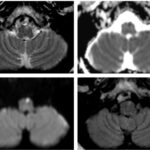
El infarto medial del bulbo se caracteriza por una lesión paramediana ventral, que compromete las pirámides bulbares, el lemnisco medial y, en casos más extensos, el núcleo o fascículos del nervio hipogloso. En resonancia magnética, estas lesiones se identifican como áreas focales hiperintensas en difusión, con disminución de la señal en el mapa ADC, generalmente con cambios sutiles o ausentes en T2/FLAIR en fases precoces.
El patrón topográfico corresponde al territorio de la arteria espinal anterior o de ramas perforantes paramedianas de la arteria vertebral, lo que permite una correlación directa entre la distribución vascular y la expresión sindrómica. La identificación precisa de esta localización en estudios de RM resulta clave para diferenciar el infarto medial del bulbo de los síndromes laterales medulares, que presentan un compromiso anatómico y vascular distinto.
Desde el punto de vista clínico, esta distribución anatómica explica la aparición de déficit motor contralateral, alteraciones de la sensibilidad propioceptiva y vibratoria, y desviación ipsilateral de la lengua, hallazgos concordantes con el síndrome bulbar medial (Déjerine).(6)
| Nivel anatómico | Topografía | Territorio vascular predominante | Estructuras / tractos
comprometidos |
Síndrome / clave de diferenciación |
| Bulbo raquídeo
(Medulla oblongata) |
Región medial – lesión paramediana ventral | Arteria espinal anterior | -Núcleo y/o fascículos del nervio hipogloso (XII).
-Lemnisco medial. -Tracto corticoespinal. |
Síndrome bulbar medial (Déjerine).
Clave: compromiso medial ventral (vs. dorsolateral). |
| Región lateral-
lesión dorso lateral |
Arteria cerebelosa posteroinferior (PICA) o vertebral | -Tracto espinotalámico.
-Núcleo ambiguo (IX y X pares craneales). -Tracto espinal del trigémino. -Pedúnculo cerebeloso inferior -Núcleos vestibulares. |
Síndrome bulbar lateral (Wallenberg).
Clave: topografía dorsolateral + territorio PICA. |
Tabla 1. Correlación anatómico-imagenológica de lesiones del bulbo raquídeo. Abreviaturas: RM, resonancia magnética; PICA, arteria cerebelosa posteroinferior.
Caso 3
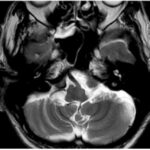
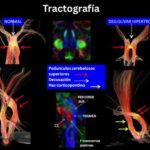
El compromiso estructural observado corresponde a una alteración del circuito dentato-rubro-olivar, cuyo daño es un mecanismo bien reconocido en la génesis de la degeneración olivar hipertrófica (DOH). En este contexto, la hiperintensidad de la oliva inferior en secuencias T2/FLAIR constituye el hallazgo imagenológico cardinal, permitiendo el diagnóstico incluso en ausencia de cambios volumétricos evidentes en fases iniciales.
La DOH representa una forma particular de degeneración transneuronal, secundaria a la interrupción de las conexiones aferentes de la oliva inferior, más frecuentemente asociada a lesiones estructurales del núcleo dentado, pedúnculo cerebeloso superior o núcleo rojo.(7) En las imágenes, este proceso se manifiesta inicialmente como un aumento de señal en T2 y FLAIR sin agrandamiento del núcleo, seguido, en fases intermedias, por incremento del volumen olivar y, finalmente, por una etapa tardía de normalización volumétrica o atrofia, con persistencia de la hiperintensidad.(8)
La identificación de estos cambios evolutivos dependientes del tiempo resulta fundamental para una correcta interpretación de las imágenes, ya que la DOH puede simular otras entidades infiltrativas o neoplásicas del tronco encefálico si no se reconoce su patrón característico.(9) En este caso, la coexistencia de una lesión estructural hemorrágica crónica en el pedúnculo cerebeloso derecho refuerza la relación causal con el compromiso contralateral de la oliva inferior.
Desde el punto de vista clínico, esta alteración anatómica se asocia clásicamente con temblor palatino sintomático, ataxia cerebelosa y alteraciones de la coordinación, aunque la expresión clínica puede ser variable y no siempre proporcional a los hallazgos en la neuroimagen.(7-9)
El ascenso desde el bulbo raquídeo hacia el puente introduce un cambio progresivo en la organización del tronco encefálico, con una mayor complejidad estructural y una disposición diferente de los núcleos de nervios craneales y de las vías largas. En este nivel, la relación espacial entre el tegmento y la porción ventral del puente adquiere un peso particular en la expresión clínica de las lesiones.
Los casos que se presentan a continuación ilustran distintos patrones de afectación pontina, permitiendo reconocer cómo variaciones sutiles en la localización de la lesión se traducen en síndromes claramente diferenciables.
Caso 4
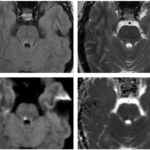
La lesión se localiza en el puente dorsomedial, en una topografía correspondiente al colículo facial, región formada por el núcleo del nervio abducens y las fibras intrapontinas del nervio facial que lo rodean. Este territorio se asocia clásicamente con el síndrome del colículo facial, caracterizado por la afectación de los circuitos oculomotores horizontales y del nervio facial.(5, 11, 12)
Desde el punto de vista anatómico, el compromiso del núcleo del VI par y de la formación reticular paramediana puede explicar la alteración de la mirada horizontal ipsilateral, mientras que la afectación de las fibras del nervio facial justifica la parálisis facial periférica ipsilateral. La ausencia de una extensión ventral significativa hacia la base del puente favorece este diagnóstico frente a otros síndromes pontinos mediales, como el síndrome de Foville, que típicamente asocia compromiso del tracto corticoespinal.(11, 12)
Caso 5
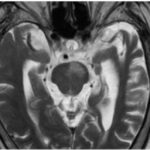
El compromiso de la porción basal del puente implica estructuras críticas, como los núcleos o fascículos de los nervios craneales VI y VII y la vía corticoespinal, configuración anatómica característica del síndrome de Millard-Gubler, un síndrome pontino ventromedial perteneciente al grupo de los síndromes alternos del tronco encefálico, descrito en asociación con múltiples etiologías y presente en todos los grupos etarios. En población joven predominan las lesiones tumorales e infecciosas, mientras que las causas vasculares, tanto isquémicas como hemorrágicas, son menos frecuentes.(13)
A diferencia de los infartos pontinos dorsales, en los que predomina el compromiso de estructuras oculomotoras y del tegmento pontino, la localización ventral observada en este caso explica la asociación de déficit motor contralateral con signos de afectación de los pares craneales ipsilaterales, patrón sindrómico clásico descrito para el síndrome de Millard-Gubler. La extensión de la lesión hacia la base del puente, sin compromiso dorsal significativo, permite diferenciar este síndrome de otras entidades pontinas mediales, como el síndrome del colículo facial o el síndrome de Foville, en los que el tegmento dorsal se encuentra involucrado.(15)
| Nivel anatómico | Topografía en RM (axial) | Territorio vascular predominante | Estructuras anatómicas comprometidas | Síndrome / clave de diferenciación |
| Puente de Varolio | Puente dorsomedial (tegmento dorsal) | Perforantes paramedianas basilar | Núcleo VI, fibras internucleares VII,
PPRF/MLF variable |
Síndrome colículo facial
Clave: dorsal puro: preserva tracto corticoespinal |
| Puente medial (tegmento) con extensión anterior | Perforantes paramedianas basilar | Núcleo VI + PPRF/MLF + fibras VII + corticoespinal (por extensión ventral) | Síndrome Foville
Clave: extensión dorsoventral sugiere compromiso corticoespinal |
|
| Puente ventromedial
(basis) |
Perforantes paramedianas basilar | Fibras VII + corticoespinal | Síndrome Raymond
Clave: ventral puro (basis) con relativa preservación dorsal |
|
| Puente dorsal superior/rostral (tegmento) | SCA/perforantes rostrales basilar (según descripción) | Pedúnculo cerebeloso superior, lemnisco medial ± trigémino | Síndrome Raymond-Cestan
Clave: dorsal superior con vías cerebelosas/lemniscales |
|
| Puente lateral caudal (tegmento lateral) | AICA/perforantes laterales basilar | Núcleos V-VIII (según extensión) | Síndrome Gasperini
Clave: lateral caudal con compromiso múltiple de pares craneales |
|
| Puente anterolateral inferior | Perforantes basilar (variable) | VII + corticoespinal | Síndrome Brissaud-Sicard
Clave: ventrolateral: patrón motor + VII, menor componente dorsal |
Tabla 2. Síndromes cruzados del tronco cerebral y su correlación anatomo-imagenológica. Abreviaturas: formación reticular pontina paramediana (PPRF); fascículo longitudinal medial (MLF); arteria cerebelosa superior (SCA); arteria cerebelosa anteroinferior (AICA). Basado en correlación anatómico-imagenológica de 5, 11, 12.
Caso 6
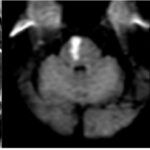
Los infartos pontinos dorsales puros, como el síndrome del colículo facial y el síndrome de uno y medio, se manifiestan en RM como lesiones confinadas al tegmento pontino dorsal, sin extensión hacia la base del puente, con preservación del tracto corticoespinal. En estos casos, el compromiso se limita a estructuras oculomotoras y fibras intrapontinas del nervio facial.(10)
En contraste, el síndrome de Foville corresponde a un infarto pontino medial con extensión dorsoventral, identificable por la afectación conjunta del tegmento dorsal y regiones ventrales del puente, lo que permite inferir el compromiso del tracto corticoespinal. Este patrón se asocia típicamente al territorio de las ramas perforantes paramedianas de la arteria basilar.
Por su parte, los infartos pontinos ventromediales puros se limitan a la basis pontis, comprometiendo predominantemente las vías corticoespinales, con relativa preservación de las estructuras dorsales.
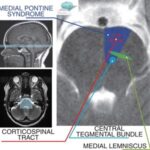
A nivel de la unión pontomesencefálica, las lesiones del tronco encefálico comienzan a mostrar patrones de afectación que ya no se ajustan estrictamente a la organización pontina clásica. La proximidad anatómica entre el puente rostral y el mesencéfalo medial favorece la aparición de lesiones continuas, cuya expresión depende del predominio rostro-caudal del compromiso.
Caso 7
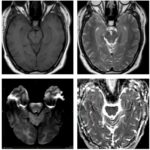
El presente caso ilustra un infarto isquémico del mesencéfalo medial, con una distribución paramediana bilateral y predominio a nivel del tegmento, acompañado de extensión caudal limitada hacia la unión pontomesencefálica. Este patrón topográfico, identificado mediante la combinación de secuencias de difusión y mapas ADC, es característico de la afectación de las ramas perforantes paramedianas del segmento distal de la arteria basilar y/o del segmento proximal de la arteria cerebral posterior, responsables de la irrigación del mesencéfalo medial, y ha sido descrito en infartos mesencefálicos mediales bilaterales dependientes de estas ramas perforantes.(5, 16)
En términos topográficos, la bilateralidad y simetría de la lesión constituyen un elemento clave para su correcta interpretación. A diferencia de los síndromes mesencefálicos alternos clásicos, como los síndromes de Weber o Benedikt, en los que el compromiso es típicamente unilateral y se extiende hacia los pedúnculos cerebrales, en este caso la lesión se encuentra confinada al tegmento medial, sin afectación significativa de las estructuras laterales, patrón previamente reportado en series imagenológicas de infartos mesencefálicos mediales.(5, 16) Este hallazgo permite descartar un patrón peduncular y refuerza el diagnóstico de un infarto mesencefálico medial.
La extensión rostro-caudal observada, con compromiso adicional del puente rostral, no debe interpretarse como la coexistencia de lesiones independientes, sino como la expresión de un territorio vascular continuo, fenómeno descrito en infartos dependientes de perforantes paramedianas largas.(17, 18) En este contexto, el análisis del eje rostro-caudal resulta tan relevante como la evaluación dorsoventral, en especial en lesiones localizadas en zonas de transición anatómica.
En este caso, la lesión se localiza predominantemente a nivel del mesencéfalo medial, con una distribución paramediana bilateral y extensión caudal limitada hacia la unión pontomesencefálica. Este patrón topográfico permite integrar los hallazgos imagenológicos dentro de un infarto mesencefálico medial y diferenciarlos de otros síndromes mesencefálicos clásicos con compromiso lateral o peduncular.(5)
Los casos presentados muestran que las lesiones isquémicas del tronco encefálico siguen patrones anatómicos reconocibles a lo largo del bulbo, el puente y el mesencéfalo. La identificación de estos patrones permite una clasificación sindrómica coherente basada en la topografía de la lesión. En conjunto, esta aproximación refuerza la consistencia del análisis anatómico como eje integrador en la evaluación de las lesiones del tronco encefálico.
Conflictos de interés
Los autores declaran no tener conflictos de interés relacionados con el contenido de este trabajo.
Bibliografía
- World Stroke Organization (2023). Global stroke fact sheet 2023. Geneva, World Stroke Organization.
- Kim, J. S. (1994). Pure lateral medullary infarction: clinical-radiological correlation of 33 patients. Stroke, 25,1409-1415.
- Zhang, X., Ma, L., Zhang, Y., Wang, Y., Zhang, B. (2015). Clinical features and functional outcomes of dysphagia in lateral medullary infarction. Neurol Sci, 36, 647-652.
- Daniels, S. K., Foundas, A. L., Iglesia, G. C., Sullivan, M. A. (2001). Lesion site in stroke and dysphagia. Dysphagia, 16, 174-182.
- Sciacca, S., Lynch, J., Davagnanam, I., Barker, R. (2019). Midbrain, pons, and medulla: anatomy and syndromes. Radiographics, 39, 1110-1125.
- Bassetti, C., Bogousslavsky, J., Mattle, H., Bernasconi, A. (1997). Medial medullary stroke: report of seven patients and review of the literature. Neurology, 48, 882-890.
- Deuschl, G., Toro, C., Hallett, M. (1994). Symptomatic and essential palatal tremor. Mov Disord, 9, 610-614.
- Goyal, M., Versnick, E., Tuite, P., Cyr, J. S., Kucharczyk, W. (2000). Hypertrophic olivary degeneration: meta-analysis of the literature and MR imaging findings. AJNR Am J Neuroradiol, 21, 1073-1077.
- Guedes Corrêa, J. F., Nóvak, E. M., Tosta, E. D., Gasparetto, E. L. (2017). Hypertrophic olivary degeneration: clinical, neuroimaging, and etiological aspects. Radiol Bras, 50, 404-409.
- Ruchalski, K., Hathout, G. M. (2012). A medley of midbrain maladies: a brief review of midbrain anatomy and syndromology for radiologists. Radiol Res Pract, 2012, 258524.
- Reynolds, C. D., Frazzitta, A. E., Rogers, S. N. (2025). The brainstem stroke atlas, part 1. Neurographics, 15, 45-57.
- Frazzitta, A. E., Reynolds, C. D., Rogers, S. N. (2025). The brainstem stroke atlas, part 2. Neurographics, 15, 144-163.
- Prasad, R., Kapoor, K., Srivastava, A., Mishra, O. (2012). Neurocysticercosis presenting as Millard-Gubler syndrome. J Neurosci Rural Pract, 3, 375-377.
- Ahdab, R., Saade, H. S., Kikano, R., Ferzli, J., Tarcha, W., Riachi, N. (2013). Pure ipsilateral central facial palsy and contralateral hemiparesis secondary to ventromedial medullary stroke. J Neurol Sci, 332, 154-155.
- Sakuru, R., Elnahry, A. G., Bollu, P. C. (2021). Millard Gubler syndrome. Treasure Island (FL), StatPearls Publishing.
- Bogousslavsky, J., Maeder, P., Regli, F., Meuli, R. (1994). Pure midbrain infarction: clinical syndromes, MRI, and etiologic patterns. Neurology, 44, 2032-2040.
- Caplan, L. R. (1980). Top of the basilar syndrome. Neurology, 30, 72-79.
- Kim, J. S. (2005). Pure midbrain infarction: clinical-radiological correlation. Stroke, 36,1234-1239.

7 comentarios en “Lesiones del tronco encefálico: correlación anatómico-imagenológica en una serie de casos”