Autora: Dra. Ana Laura Zambrano (Centro médico Diagnóstico Científico Integral, Capital Federal, Argentina)
Tutora: Dra. Marta Luján Kura (Centro médico Diagnóstico Científico Integral, Capital Federal, Argentina)
1. Introducción
Los sarcomas son un grupo grande y diverso de tumores malignos de origen mesenquimal. La organización mundial de la salud (OMS) los divide en dos categorías grandes: Sarcomas de tejidos blandos y los sarcomas óseos. (Cuadro 1).
Comparados con otros tipos de neoplasias malignas, los sarcomas de partes blandas son tumores relativamente raros. Se estima que cada año se diagnostican aproximadamente 5000 casos en el mundo según los datos de la OMS, lo que representa un 1% de todas las neoplasias diagnosticadas de novo en el mismo periodo.
El liposarcoma supone del 9.8 al 18% del total de sarcomas de partes blandas en el mundo, siendo la segunda variante histológica en frecuencia de estos tumores; su incidencia se sitúa por detrás únicamente de la del fibrohistiocitoma maligno (FHM).
En series locales se presenta con una frecuencia del 1.8 al 16,3 % diagnosticado en el ámbito público de salud y en los servicios privados del 3,8 al 12,6 % de frecuencia y su incidencia se sitúa por detrás únicamente de la del Leiomiosarcoma (LMS) (Tabla 2).
El liposarcoma (LPS) es el tipo histológico más frecuente suponiendo alrededor del 50% de los sarcomas retroperitoneales (SRP) y está dividido en los subtipos histológicos bien diferenciado (LPS BD), mixoide/células redondas (LPS Mix), pleomorfo (LPS Pl), desdiferenciado (LPS DD) y mixto. Desde un punto de vista clínico, estos tumores son difíciles de detectar debido a su crecimiento silente. Así, pueden alcanzar un tamaño desproporcionado, comprimiendo las estructuras vitales cercanas.
Haciendo referencia puntual al subtipo mixoide este tiene una frecuencia del 3,6 y el 6 % en series de estudios retrospectivos locales (Tabla 2).
El liposarcoma es un tumor derivado de células primitivas capaces de diferenciarse hacia tejido adiposo (el que compone las grasa de debajo de la piel, y que también se encuentra alrededor de varios órganos y en torno a los músculos).
Los sarcomas de tejidos blandos afectan a todos los grupos etarios y se pueden desarrollar en múltiples ubicaciones.
En series norteamericanas su incidencia es del 1% de la totalidad de tumores malignos. Aproximadamente el 60% se originaba en alguna extremidad (más común en la región del muslo), 19% en las paredes del tronco, 15% en el retroperitoneo y 9% en cabeza y cuello.
Hay muy pocos datos epidemiológicos locales y regionales con respecto a los SPB del adulto.
Constituyen un raro y heterogéneo grupo de tumores malignos originados en el tejido conectivo, con formas muy diferenciadas y de crecimiento muy lento, hasta otras de alta actividad mitótica y letal en corto tiempo y que comprende más de 100 subtipos histológicos diferentes según algunos autores. En su mayoría derivan de una célula mesodérmica toti potencial, que puede diferenciarse en cualquier tipo celular propio del tejido conectivo maduro (fibroblastos, adipocitos, células musculares, etc.).
Otros tumores, como por ejemplo malignos de la vaina de nervio periférico, si bien derivan del ectodermo, por sus similitudes clínicas y biológicas se incluyen por convención dentro de los SPB. Si bien pueden originarse en cualquier lugar del organismo donde exista tejido conjuntivo, estos tumores se observan en más de la mitad de los casos en las extremidades.
En general, son poco estudiados en lo que respecta a su biología molecular y opciones terapéuticas.
Debido a la baja frecuencia y al diferente comportamiento de estos subtipos tumorales entre sí, es muy complicado reclutar suficientes pacientes en el marco de ensayos clínicos que permitan arrojar conclusiones robustas sobre los tratamientos.
El manejo de esta afección requiere la participación de un equipo multidisciplinario experimentado, desde la planificación de la biopsia, pasando por el diagnóstico anatomopatológico, hasta el tratamiento local o sistémico.
El conocimiento sobre las enfermedades debe ser el punto de referencia para planear acciones que mejoren el diagnóstico y tratamiento de las mismas.
2. Objetivos
Objetivos generales
- Complementar con la bibliografía reportada, los aspectos clínicos y médicos sobre la patología del Liposarcoma mixoide.
- Detallar las características clínico- epidemiológicas de esta patología según la literatura y destacar puntos en común con el caso a describir.
- Conocer los diferentes métodos de imagen que nos facilitan el diagnóstico de los sarcomas del liposarcoma mixoide, y determinar cuál presenta mayor sensibilidad y especificidad según la bibliografía.
Objetivos específicos
- Reconocer cuales métodos de imagen son más útiles para el diagnóstico del Liposarcoma de variante mixoide en correlato con las imágenes presentadas del caso clínico y describir las características clínicas del paciente pesquisado de la casuística del Centro de Diagnóstico Científico Integral.
3. Materiales y métodos
Los datos principales del caso clínico son recurso del Centro de Diagnóstico Científico Integral.
Se usó como complemento la bibliografía de artículos publicados por revistas reconocidas de especialidades de oncología, cirugía oncológica, y radiológicas, de países como España, Estados Unidos de Norteamérica, Cuba, Chile y Argentina , por medio de los motores de búsqueda de The National Library of Medicine, RadioGraphics – RSNA Publications Online y Cochraine library, usando las palabras clave como “Liposarcoma mixoide TC RM”, “Malignant and Benign Musculoskeletal Tumors”, “Liposarcoma”, “Musculoskeletal Masses”, “Radiologic Pathologic Correlation”, principalmente revisiones desde el 2014 al 2019, para realizar la revisión de la literatura.
4. Desarrollo del tema
Presentación del caso clínico
Se presenta a una paciente de sexo femenino, de 50 años de edad, bajo manejo de oncología por diagnóstico previo de Liposarcoma de estirpe mixoide. Diagnosticada en 2007 por presentar masa palpable indolora en región posterior de muslo izquierdo, la cual es biopsiada y resecada junto con la totalidad del paquete isquiotibial izquierdo. Reporte anatomopatológico liposarcoma mixoide-redondo celular. Recibiendo quimioterapia y radioterapia.
En 2011 presenta recidiva local de la enfermedad sin evidencias de diseminación a otras zonas, recibe esquema de quimioterapia y radioterapia. Controles posteriores no detectaron alteraciones.
En 2016 se detecta recidiva a nivel de 9na costilla y región retroperitoneal retropancreática por lo que se reinteviene quirúrgicamente y se extirpan focos señalados. Recibiendo RT y QT posterior. El reporte de anatomopatología informa ¨Liposarcoma mixoide con extensas áreas de necrosis, hialinización y un componente redondo celular del 20% (grado II-III histológico) ¨ con márgenes limpios en las dos muestras.
Luego en 2019, en marzo control tomográfico sin cambios, sin embargo en junio de este mismo año debuta con dolor abdominal en epigastrio por lo que consulta al clínico quien solicita RM contrastado de abdomen dado sus antecedentes. Esta reporta una imagen ocupante de espacio heterogénea, sólido-quística en íntima relación con la cabeza pancreática 38 x 15 x 22 mm, y PET TC 18FDG que confirma foco hipercaptante en esta zona. Dado el hallazgo se somete a comité oncológico y se interviene quirúrgicamente. El estudio de anatomopatología informa 17/07/2019 liposarcoma mixoide grado II histológico.
Se realizan estudios de control tomográfico y ecográfico postquirúrgicos reportando cambios postquirúrgicos sin otro hallazgo de mención. Centellograma en noviembre del 2019 informa baja probabilidad de secundarismo en esqueleto.
El 2020 en marzo se realiza PET TC 18FDG que reporta dos focos hipercaptantes en rodilla izquierda en relación a estructuras ligametarias, resolución del foco previo encontrado cerca de la cabeza del páncreas y en cuanto al aspecto tomográfico del resto de estructuras no se reportan cambios significativos.
Es recibida en DCI para realizarse sus estudios de control en julio RM de muslo región glútea izquierdas, ecografía de partes blandas y TC de tórax abdomen y pelvis con contraste.
En la actualidad la paciente continua con su control oncológico y manejo de quimio y radioterapia conjunta como terapéutica de primera línea.
Estudios de imagen
11-03-2020 (IMAXE) Estudio PET- TC (cuerpo entero incluyendo cabeza y miembros inferiores)
Se ha efectuado un estudio PET –TC con un equipo hibrido y TC multislice.
Las imágenes obtenidas expresan correlación anatomo- metabólica.
Se adquirieron imágenes a partir de los 60 minutos de la administración del radiofármaco, obteniéndose cortes tomográficos en los 3 planos e imágenes volumétricas y fusión de ambas modalidades.
Radiofármaco: F18-FDG (fluoro deoxi-glucosa). Dosis 10 mCi.
Hallazgos PET- TC
El examen PET-TC realizado muestra imágenes de concentración patológica del radiotrazador en:
- Nódulo hipermetabólico con densidad de partes blandas, ubicado por detrás y debajo del sector lateral de la rótula izquierda. Mide 18,4 mm. SUV 12,2.
- Foco hipermetabólico proyectado sobre una pequeña imagen con densidad de partes blandas, ubicada en el margen póstero-medial de la meseta tibial izquierda. Se relaciona con las estructuras ligamentarias y tendinosas adyacentes. Mide 11,0 mm. SUV 3,3.
No se observaron otras imágenes hipermetabólicas en el resto del examen corporal total.
Hallazgos en TC no hipermetabólicos en PET
- Clips quirúrgicos en el epigastrio, acorde a los antecedentes.
- El examen de los campos pulmonares muestra una imagen subpleural, de aspecto secuelar en el segmento anterior del lóbulo superior derecho y engrosamientos pseudonodulares, también de aspecto secuelar en la cisura mayor. Aislados nodulillos subpleurales a predominio del lóbulo inferior izquierdo, ninguno supera los 5 mm.
- Imagen compatible con un puente óseo entre el sector posterior de 7° y 8° arcos costales derechos y solución de continuidad del sector lateral del 10° arco costal homolateral.
- El hígado presenta una imagen de aspecto quístico en el segmento VIII. Mide 5 mm.
- Bazo y glándulas suprarrenales no muestran alteraciones
- Páncreas con cambios postquirúrgicos.
- Ambos riñones de forma y tamaño conservados.
- Examen de encéfalo no muestra alteraciones.
- No se observan otras particularidades.
Comparación con estudios previos:
- De la comparación con el PET-TC previo de fecha 06/06/2019, se observa:
- Resolución de la imagen descripta por delante del cuello pancreático, acorde a los antecedentes quirúrgicos.
- Persiste con leve aumento del metabolismo la imagen nodular hipermetabólica por detrás de la rótula izquierda
- Persiste foco hipermetabólico proyectado sobre una pequeña imagen con densidad de partes blandas, ubicada en el margen póstero-medial de la meseta tibial izquierda.
- No presentan modificaciones significativas las opacidades nodulillares pulmonares bilaterales, a predominio del lóbulo inferior izquierdo.
Controles de imágenes que se realizaron en DCI por métodos de ecografía en lecho quirúrgico de muslo izquierdo (31-07-2020) en la que observa en topografía de la cara posterior del tercio distal del muslo izquierdo, la presencia de imagen focal de baja ecogenicidad de aspecto sólido, márgenes circunscriptos y vascularización negativa al estudio con Power Doppler de 18 x 7 x 14 mm cuyo centro se ubica a 29 mm de la superficie cutánea. (Fig. 1, Fig. 2, Fig. 3) de la cual se solicita complementar con estudio de resonancia magnética nuclear de pelvis y pierna izquierda.
Resonancia magnética nuclear de pelvis y pierna izquierda (28-07-2020) en la que persiste la imagen localizada por ecografía de características, describiéndose:
En el tercio medio del muslo izquierdo (Fig. 11, Fig. 12, Fig. 13 y Fig. 14), ocupando el espacio intermuscular posterior, adyacente al paquete vasculonervioso de este lado, se reconoce una imagen ovalada de contornos netos que:
- Mide 13 mm.
- Emite señal hiperintensa en secuencias T2 e hipointensa en secuencias T1 con marcado refuerzo posterior a la administración de contraste endovenoso.
- Restringe al estudio con secuencias de difusión. Constituye un hallazgo de aspecto inespecífico sin poder descartar su vinculación a la patología de base.
- Sugerimos su estricto control evolutivo.
No se advierten otras áreas de refuerzo patológico tras la administración de contraste endovenoso ni focos restrictivos al estudio con técnica de difusión.
- En el hueso ilíaco izquierdo, por detrás de la espina ilíaca antero-superior, se observa un área focal hipointensa en T1, heterogénea en T2 e hiperintensa en secuencias STIR (Fig. 15, Fig. 16, Fig. 17 y Fig. 18).
- Teniendo en cuenta los antecedentes de la paciente y para su adecuada caracterización, sugerimos complementar con centellograma óseo a fin de descartar un probable foco secundario.
Se realizada una TC de tórax, abdomen y pelvis antes y después de administrar contraste por vía endovenosa con reconstrucción multiplanar (31-07-2020). El estudio fue efectuado teniendo en cuenta las indicaciones de la orden médica. (Nota: se toma como referencia el PET TC previo de marzo/2020). El examen realizado muestra:
Tórax
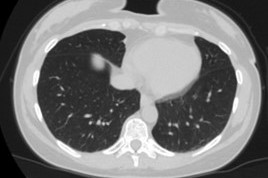
- Aislados nodulillos no calcificados de distribución subpleural bilateral, ninguno de ellos supera los 5 mm de diámetro (Fig. 4, Fig. 5, Fig. 6 y Fig. 7).
- Finos engrosamientos pleurales biapicales de intercisural es con particular compromiso de la cisura mayor del lado derecho, todos ellos de aspecto secuelar.
- Dichos hallazgos muestran características semejantes al examen de referencia.
- Mediastino y axilas libres de adenomegalias.
Abdomen y pelvis
- Hígado de forma y tamaño conservado. Quiste simple de 5 mm en lóbulo hepático derecho. (Fig. 8)
- En el segmento hepático VI/VII se observa una pequeña imagen redondeada que muestra realce progresivo con la administración de contraste llegando a homogenizar con el resto del parénquima en secuencias tardías. Mide 5mm y es compatible en primer término con un hemangioma. (Fig. 8)
- Cambios postquirúrgicos en el epigastrio, lesión céfalocorporal del páncreas ya descrita previamente. (Fig. 10)
- El bazo, glándulas adrenales y riñones muestran forma y tamaño conservado.
- Los riñones concentran y excretan adecuadamente el contraste endovenoso.
- Mesenterio y retroperitoneo libres de adenomegalias.
- Escasa cantidad de líquido libre en fondo de saco.
- Vejiga de paredes finas con adecuada repleción.
- Los restantes cortes que pasan por la pelvis no portan otras particularidades.
- Se reconoce un puente óseo que comunica el sector proximal del séptimo y octavo arco costal del lado derecho.
- Resección quirúrgica de los 2/3 anteriores del décimo arco costal derecho acorde a los antecedentes. (Fig. 9)
- El resto del estudio de las estructuras óseas no aporta otras particularidades.
Se realiza una RM de muslo izquierdo con contraste (30-09-2020) y con cortes en diversos planos. Se utilizaron secuencias que estudian los tiempos de relajación tisular T1, T2, STIR, difusión y secuencias con contraste. El estudio fue efectuado de acuerdo a las indicaciones de la orden médica. (Nota: se compara con la RM previa de julio/2020). El examen realizado muestra:
- En el examen actual, persiste y sin cambios con respecto al estudio de referencia la formación focal ovalada de 13mm. (Fig. 19, Fig. 20, y Fig. 21)
- Muestra refuerzo con el contraste y restricción al estudio con técnica de difusión sin caída significativa de su señal en el mapa ADC.
- Si bien podría corresponder a un área secuelar, sugerimos su control evolutivo teniendo en cuenta sus antecedentes.
5. Revisión bibliográfica
Liposarcoma mixoide
Es el segundo tipo más común de los liposarcomas (20% al 50%) y corresponde al 10% de todas las neoplasias de tejidos blandos.
Previamente, los liposarcomas mixoides y de células redondas eran considerados distintos subtipos histológicos. En la actualidad la Organización Mundial de la Salud los agrupa en su clasificación de manera combinada como “liposarcoma mixoide” representando estos dos subtipos. (Tabla 2)
Los liposarcomas no muestran predilección por algún género. Las lesiones ocurren con mayor frecuencia en pacientes aproximadamente una década más jóvenes que aquellos que se ven afectados por otros tipos de liposarcoma, con un pico de prevalencia entre la cuarta y quinta década de la vida. Son extraordinariamente raros en pacientes en la primera década de vida. Sin embargo el liposarcoma mixoide es el tipo más común de liposarcoma que afecta a los niños representando un 76% de lesiones sarcomatosas en pacientes entre los 10 y los 16 años.
Los liposarcomas mixoides de las extremidades es la manifestación más frecuente deriva de tejidos intermusculares (70 a 80% de los casos) y con menos frecuencia derivan del tejido muscular o subcutáneo. Estas lesiones predominantemente afectan las extremidades inferiores en un 75 a 80% de los casos, particularmente el muslo a nivel medial y la región poplítea. Otras locaciones menos frecuentes incluyen los tobillos, la región inguinal y glútea. Las lesiones de miembros superiores representan el 5% de todas las lesiones y las retroperitoneales 8%.
Desde un punto de vista clínico, estos tumores son difíciles de detectar debido a su crecimiento silente. Así, pueden alcanzar un tamaño desproporcionado, comprimiendo las estructuras vitales cercanas. La recurrencia locorregional es la principal causa de mortalidad (Fig. 4).
Las metástasis a distancia en el momento del diagnóstico son raras; con mayor frecuencia se localizan en el pulmón o el hígado y su ocurrencia se ha cifrado en alrededor del 10%.
Otro punto de interés fue la influencia de diferentes factores clínicos en la recurrencia precoz.
La cirugía es el tratamiento más efectivo en los SRP. Obtener márgenes sin afectación tumoral es el principal objetivo a alcanzar, llegándose a realizar grandes resecciones multiviscerales para garantizar tal fin.
El tamaño de estos tumores y su relación con las diferentes estructuras de la cavidad abdominal dificultan la escisión total con márgenes libres de afectación tumoral (ilustraciones 1 y 2).
El uso de la radioterapia no está exento de controversia. Tradicionalmente, se ha considerado útil con el control local asociado a la cirugía; sin embargo, deben desarrollarse estudios prospectivos que respalden su uso. La quimioterapia se ha limitado a tumores recurrentes y metastásicos debido a su efectividad limitada.
El comportamiento de los LPS retroperitoneales esta poco estudiado. En la literatura suele incluirse en estudios donde se agrupa, bien con LPS de otra localización, bien con el global de tumores retroperitoneales debido a su baja frecuencia.
Etiología
El 90% de las lesiones de liposarcomas de estirpe mixoide tienen una traslocación cromosómica característica que conduce a la fusión de los genes DDIT3 y FUS en las regiones cromosómicas 12q13 y 16p11. La consecuencia es la creación de una proteína híbrida FUSDDIT3 que promueve la transformación maligna mediante la desregulación de la transcripción del ARN y de este modo alterando la diferenciación de adipocitos y el control del ciclo celular.
Característica histológicas
Macroscópicamente son lesiones bien circunscritas, multinodulares, de color café marrón y de apariencia y consistencia gelatinosa. A veces coexisten áreas amarillentas compuestas por adipocitos maduros o áreas con aspecto de carne de pescado, correspondientes a los focos de las células redondas.
Su apariencia varía dependiendo del grado de células mixoides y redondas en su composición. (Tabla 1)
Las lesiones de composición predominantemente mixoide son de aspecto gelatinoso, mientras que las lesiones con áreas focales de células redondas forman nódulos blancos opacos.
Lesiones con un componente predominante de células redondas tienen aspecto blanquecino, de apariencia no específica similar a aquel que se encuentra en los sarcomas de tejidos blandos. Son generalmente considerados de grado intermedio cuando su componente es predominantemente mixoide y de un alto grado si su componente de células redondas supera substancialmente al primero. (Fig. 2)
El liposarcoma mixoide presenta un patrón de crecimiento nodular, hipocelular, con vasculatura plexiforme en una matriz mixoide, a menudo produce un patrón con lagos de mucina llamado linfangioma-like. Las células son pequeñas, fusiformes, con escaso citoplasma y un núcleo oval, que alternan con lipoblastos atípicos en diversos estadios de maduración. El liposarcoma mixoide con células redondas presenta escasa matriz mixoide, disminución de la trama vascular, hipercelularidad y mayor grado de atipia. (Fig. 3)
El análisis histológico del LSM consiste en lóbulos bien diferenciados de tejido mixoide, un característico y delicado árbol capilar; un componente uniforme de células mesenquimales con cantidades variables de lipoblastos monovacuolados o bivacuolados, particularmente en la periferia de los lóbulos. Pueden observarse áreas alternadas de adipocitos maduros rodeado por matriz mixoidea y también, también áreas de hemorragia.
Las áreas con predominio componente de células redondas incrementan la celularidad en este grupo de lesiones. Estas áreas están caracterizadas por capas sólidas de células redondas primitivas con reemplazo de estroma mixoide y patrón vascular típico. Los componentes mixoides y de células redondas, a menudo se encuentran yuxtapuestos, con áreas de alta actividad mitótica y focos de necrosis en los componentes de células redondas.
A menudo esto produce una gradual transición de los componentes mixoides a estas áreas de células redondas, que en apariencia nos sugiere un correlato histológico de continuidad de estas lesiones.
Liposarcoma mixoide es genéticamente caracterizado por la translocación recíproca de t(12;16)(q13;p11). Este componente genético está presente en más del 90% de los casos. Es a su vez altamente específico y sensible desde que no está asociado con otras translocaciones como las de los mixofibrosarcomas o del liposarcoma bien diferenciado con variante mixoide.
Clasificación
La clasificación de Evans distingue tres grados, con diferente evolución clínica y pronóstico:
- Grado I, < 5 % de células redondas. El pronóstico es bueno, las recidivas locales se presentan en 50 % de los pacientes y la supervivencia es de 70 % a los 10 años.
- Grado II, entre 5 y 25 % de células redondas. La evolución es difícil de predecir
- Grado III, > 25 % de células redondas. Las lesiones son catalogadas como sarcomas de alto grado, con alta capacidad de dar metástasis.
Diagnóstico diferencial
El diagnóstico diferencial histopatológico de esta lesión incluye una amplia gama de lesiones, tales como neoplasias adipocíticas benignas (lipoblastoma y lipoma condroide), tumores mesenquimales mixoides benignos (mixoma intramuscular) y malignos (mixofibrosarcoma, condrosarcoma mixoide, dermatofibrosarcoma protuberans mixoide).
Caracterización por imágenes
En radiografías LSM puede aparentar tejido normal, pero con mayor frecuencia suele revelarse como una masa de tejido blando de aspecto no específico. Presenta calcificaciones con menor frecuencia que el liposarcoma bien diferenciado (LSBD), así como el aspecto radiolúcido de la grasa también se muestra con menor frecuencia en comparación al LSBD, debido al menor volumen de tejido adiposo en estas lesiones.
Ultrasonográficamente se revela como una masa compleja de márgenes definidos, de aspecto hipoecogénico pero alternado con áreas sólidas, con refuerzo acústico posterior.
A pesar de que el tejido adiposo no puede ser específicamente identificado por este método, en muchos casos, la evaluación ultrasonográfica puede sugerirnos el diagnostico, en combinación con TC y RM como un complemento, descartando lesiones quísticas, y en el caso de procedimientos de biopsia, con técnicas ecoguiadas.(Ilustración 4).
En casos de LSM de ubicación poplítea donde puede ser confundido con un quiste de Baker, la evaluación por US resulta crucial para determinar la morfología del quiste de Baker verdadero, que posee un contenido líquido que se extiende finamente en la unión de los tendones del gastrocnemio y semimembranoso (Ward y cols) y que son de presentación superficial, estas características descartan el diagnostico de LSM.
Hablando de TC y RM LSM a menudo tiene una presentación más típica, caracterizada por ser una lesión de tamaño grande, multilobulada bien definida de origen intermuscular. Su alto contenido de agua se traduce en imágenes de TC que se muestran densidad intermedia, y en MR baja señal en imágenes ponderadas en T1, y marcada hiperseñal en el T2 (Ilustración 3).
A menudo un signo patognomónico es la presencia de tejido adiposo visualizado dentro de la masa, que se puede evidenciar con secuencias Fat-Sat , constituye un 10% de la composición de la lesión, y se agrupa generalmente (90-95% Murphy y cols.) en forma de septos (patrón linear) o a manera de sutiles nodulillos dentro de la lesión (Ilustración 5).
Otro diagnostico diferencial por imágenes es el Mixoma que a menudo se muestran de presentación intramuscular, rodeados por tejido atrófico y edema, manifestaciones que no son comunes en el LSM.
Los LSM realzan al contraste en MR, esto los distingue fácilmente de lesiones quísticas. El realce periférico se presenta en el 60% de los casos, realce central y difuso con una menor proporción. (Tateishi y cols.)
Los LSM con mayor proporción de celular redondas pueden evidenciar áreas de relativa menor cantidad de líquido en US, CT, y MR.
Estas áreas presentan características inespecíficas, pero se manifiestan como un tejido solido de ecogenicidad intermedia, en TC muestran densidades similares a las del tejido muscular, y en MR señal intermedia en imágenes ponderadas en el T1 y T2. Series de estudios reportan como signo de mal pronóstico la ausencia de septos finos, engrosamiento capsular y el acusado refuerzo postcontraste inmediato.
Los hallazgos de resonancia magnética son más específicos para un LSM puro, manifestándose como una lesión encapsulada con señal hipointensa en T1 y marcada hiperintensidad en T2. Se puede asemejar a un mixoma intramuscular, y en algunos casos, la apariencia puede incluso asemejarse a una lesión quística. Sin embargo, diferente a las lesiones quísticas, los LSM muestran un marcado realce en su estructura, algunas veces heterogéneo. Adicionalmente la identificación de componentes grasos asociados ayuda en la diferenciación.
Los LSM de alto grado tienden a tener una presentación atípica con intensidad de señal heterogénea en las imágenes ponderadas en T1 y T2 debido a formaciones de células redondas mezclados con la matriz mixoide y células grasas. Este componente de células redondas tiene señal intermedia en las ponderaciones del T2 a diferencia del componente mixoide, resultando el realce heterogéneo de la lesión. A pesar de que las características de la RM no son específicas, los hallazgos de imágenes de invasión vascular u ósea, circunscripción a estructuras vasculares, ausencia de pseudocapsula y presencia de necrosis tumoral son hallazgos más comúnmente asociados a los LSM de alto grado.
La utilidad de la tomografía de positrones (PET) con flúordeoxiglucosa (FDG) está reconocida para carcinomas de alto grado o menos diferenciados tienen alta utilización de glucosa y FDG, por su expresión de transportadores GLUT superficiales; por otra parte, los sarcomas pueden presentar captación variable con utilidad no bien establecida pues las publicaciones cuentan con muestras pequeñas y/o heterogéneas. Existe alto rendimiento para sarcomas óseos, pero menos información en otros tipos y localizaciones. El estudio PET con FDG demostró utilidad para diagnóstico y control de terapia, en sarcomas de alto grado y menos diferenciados, de adultos y niños; en la pesquisa de nuevas lesiones, lo que podría cambiar el pronóstico y manejo.
Tratamiento y pronóstico
El tratamiento de elección del LSM es la escisión quirúrgica total de la lesión. En casos en los que no es posible resecar en su totalidad de márgenes debido al tamaño, infiltración periférica de órganos no resecables o proximidad a troncos vasculares y nerviosos principales, a menudo, la radioterapia es utilizada para reducir la recurrencia local. La quimioterapia adyuvante (doxorrubicina y dacarbazina) en combinación también ha probado beneficios en el tratamiento.
La incidencia de enfermedad metastásica se incrementa significativamente en pacientes cuyo LSM contiene mayor proporción de células redondas en el estudio histopatológico Grados II y III).
Otros factores que favorecen el mal pronóstico son la edad superior a 45 años, y la presencia de focos necróticos en la histología de la lesión. (Tabla 2. Factores asociados a la recurrencia).
La supervivencia 5 años en pacientes con LSM se estima entre el 47-77%.
Contrario a otros subtipos de liposarcomas, las lesiones de estirpe mixoide tienen fuerte predilección por tejidos extrapulmonares como retroperitoneo, tórax (pared torácica, pericardio, pleura) y pelvis, para metastatizar. Estas lesiones metastásicas a menudo mantienen sus características de tejido mixoide en la imágenes.
La incidencia de metástasis óseas se han reportado en un 17%, superior incluso a las metástasis pulmonares (14%) de los pacientes.
6. Discusión
Los liposarcomas constituyen el grupo más numeroso de sarcomas del adulto, y propiamente el LSM representa casi 20 % de las neoplasias en este grupo. Sus criterios diagnósticos han sido bien establecidos, como se refleja en la clasificación actual de la Organización Mundial de la Salud.
Se localizan principalmente en las extremidades inferiores, predominan en muslo, glúteo y hueco poplíteo. Rara vez se presentan en tejido subcutáneo o retroperitoneo. Se han informado localizaciones poco frecuentes como pulmón, corazón, órbita y columna vertebral. La ubicación del liposarcoma en este último lugar ha sido informada en la literatura mundial solo en dos pacientes.
Anteriormente, los liposarcomas eran clasificados por la Organización Mundial de la Salud en dos subtipos histológicos: mixoides y de células redondas, sin embargo, la evidencia clínica, morfológica y citogenética apoya claramente la existencia de un espectro único de lesiones en el que los liposarcomas mixoides y de células redondas representan una entidad bien y pobremente diferenciada, respectivamente. Ambos presentan la translocación t(12; 16) (q13;p11) FUSDDIT3.
En las tomografías computarizadas, los liposarcomas se observan como lesiones muy variadas, aunque típicamente son masas de densidad intermedia, en algunos casos heterogéneas, cuyo valor de atenuación varía e incluso es superior al de la grasa normal en las lesiones muy mixoides e inferior al de los tejidos blandos circundantes.
La resonancia magnética es el estudio de elección para definir los tumores de tejidos blandos, delinear su ubicación anatómica y llevar a cabo una biopsia satisfactoria, así como para planear el procedimiento quirúrgico.
El tratamiento de elección es la resección amplia y completa, siempre que las estructuras adyacentes lo permitan. La cirugía se complementa con radioterapia adyuvante, que ha demostrado mejorar el control local y la tasa de supervivencia y, en ocasiones, con la quimioterapia con doxorrubicina y dacarbazina.
El liposarcoma mixoide puro en general tiene un alto riesgo de recidiva local (50 %) y de metástasis (20 %). Presenta tendencia a hacer metástasis a sitios extrapulmonares, tejidos blandos, retroperitoneo, mediastino, pared torácica, superficie peritoneal y pericardio.
La tasa de la supervivencia media es de 77 % a los cinco años y de 47 % a los 10 años y está determinada por la resección local. Después de la recurrencia, el curso clínico por lo general es tórpido.
Características clínicas significativas
En nuestro caso, la evolución y el pronóstico de la paciente está marcado por el alto grado de la lesión en la estatificación patológica del 2016, un rasgo representativo de este grupo son los múltiples episodios de recurrencias.
En coincidencia con los artículos investigados se destaca que la edad de la paciente concuerda con el grupo etario de mayor incidencia.
La valoración de lechos quirúrgicos previos se realizó por medio de ecografía, TC, y RM. Tomando en cuenta que en la literatura actualizada se hace especial énfasis en los avances de las diferentes técnicas y ponderaciones para llegar a un control seguro de la evolución de las lesiones.
Otras lesiones a tener en cuenta son las lesiones hipercaptantes localizadas por el PET TC en rodilla izquierda, las que se continúan observando en los estudios posteriores de RM y TC, por lo que se realiza su respectiva comparativa en los informes imagenológicos de nuestro centro.
El estudio PET con FDG demostró utilidad para diagnóstico y control de terapia, en sarcomas de alto grado y menos diferenciados, de adultos y niños; en la pesquisa de nuevas lesiones, lo que podría cambiar el pronóstico y manejo.
Contribuyen a la estabilidad de los hallazgos el hecho de que hasta la actualidad la paciente continua con su control oncológico y manejo de quimio y radioterapia conjunta como terapéutica de primera línea.
7. Conclusiones
Los liposarcomas mixoides muestran una clara preferencia a desarrollar metástasis en otros tejidos blandos a sitios extrapulmonares, tejidos blandos, retroperitoneo, mediastino, pared torácica, superficie peritoneal y pericardio.
Este es un hecho que ya es conocido desde hace tiempo, por lo que en los protocolos de seguimiento de estos tumores se incluye, además de la TC torácica, la TC abdominopélvica representando el método más sensible en la detección de estas lesiones en primera instancia. Además, se debe de incluir el TC de abdomen y pelvis la detección y seguimiento de estos tumores.
Se ha demostrado la utilidad de la resonancia magnética, en la actualidad es el estudio de elección para definir los tumores de tejidos blandos (8, 9, 10 y 11), delinear su ubicación anatómica y llevar a cabo una biopsia satisfactoria (5, 6), así como para planear el procedimiento quirúrgico.
La inclusión de la difusión en las series de estudios gana cada vez más espacio como herramienta para definir los tumores de tejidos blandos, delinear su ubicación anatómica, determinar su celularidad y composición, así como para planear el procedimiento quirúrgico, y estrategias de tratamiento posterior (4).
En correlato el caso citado en esta revisión, se confirma que la incidencia de enfermedad metastásica se incrementa significativamente en pacientes cuyo LSM contiene mayor proporción de células redondas en el estudio histopatológico Grados II y III).
8. Bibliografía
- Dres Andrés Julián Vanrell, Juan Peralta, Andrés Saez, Alexander Ballesteros Ospina Liposarcoma retroperitoneal gigante: a propósito de un caso. Revista de la Asociación Médica Argentina, Vol. 131, Número 1 de 2018.
- Área de Investigación, Asociación Argentina de Oncología Clínica. Registro argentino de sarcomas de partes blandas del adulto. Análisis retrospectivo de los datos obtenidos durante dos años en una institución pública y tres instituciones privadas. 2017.
- Félix Báez Sarría, MSc. Tomás Lázaro Rodríguez Collar, MSc. René Santiago Borges Sandrino, MSc. Bárbara Mercedes Paula Piñera. Liposarcoma mixoide retroperitoneal. Revista Cubana de Medicina Militar vol.42 no.4 Ciudad de la Habana sep.-dic. 2013.
- Mark J. Kransdorf, MD, Mark D. Murphey, MD. Imaging of Soft-Tissue Musculoskeletal Masses: Fundamental Concepts. RadioGraphics 2016; 36:1931–1948.
- Mark D. Murphey, MD. Lynn K. Arcara, MD. Julie Fanburg-Smith, MD. Imaging of Musculoskeletal Liposarcoma with Radiologic-Pathologic Correlation. RadioGraphics 2015; 25:1371–1395
- Gunjan M. Senapati, MD Robert G. Sheiman, MD Salwan Almashat, MD Jeffrey D. Goldsmith, MD. Pleomorphic Liposarcoma of the Inferior Vena Cava. RadioGraphics 2015; 35:269–274
- Pushpender Gupta, MBBS Tommy A. Potti, MD Scott D. Wuertzer, MD Leon Lenchik, MD David A. Pacholke, MD. Spectrum of Fat-containing SoftTissue Masses at MR Imaging: The Common, the Uncommon, the Characteristic, and the Sometimes Confusing. RadioGraphics 2016; 36:753–766.
- Sandy Lucero Granados-López, Juana Sonia Tavares-García, Alberto Pérez-Contreras. Liposarcoma mixoide en columna vertebral lumbosacra Informe de un caso clínico. Reportes breves. Rev Med Inst Mex Seguro Soc. 2013;51(5):588 91.
- Juan Manuel Sánchez-Hidalgo, Sebastián Rufián-Peña, Manuel Durán-Martínez,, Pedro Lopez-Cillero, Javier Briceño-Delgado. Factores de riesgo implicados en la recurrencia precoz del liposarcoma retroperitoneal. Revista de cirugía general. Elsevier. 96. Núm. 9.páginas 568-576. Noviembre 2018.
- Jonelle M. Petscavage-Thomas, MD, MPH Eric A. Walker, MD Chika I. Logie, MD Loren E. Clarke, MD Dennis M. Duryea, DO Mark D. Murphey, MD. Soft-Tissue Myxomatous Lesions: Review of Salient Imaging Features with Pathologic Comparison. RadioGraphics 2014; 34:964–980.
- Angela D. Levy, MD Maria A. Manning, MD Waddah B. Al-Refaie, MD Markku M. Miettinen, MD. Soft-Tissue Sarcomas of the Abdomen and Pelvis: RadiologicPathologic Features, Part 1— Common Sarcomas. RadioGraphics 2017; 37:462–483.
Agradecimientos
A mi familia, por ser mi soporte y motivación de ser más para servir mejor.
Mi eterno reconocimiento a la labor de docentes por la entrega diaria de conocimiento, sin duda me llevo gratos recuerdos de cada uno.
Al centro médico Diagnóstico Científico Integral por recibirme durante estos años y compartir experiencias que enriquecieron mi práctica diaria.